Gerb erozívna forma 2 stupeň aktivity. Gerb (gastroezofageálna refluxná choroba). I. Pažerákové ťažkosti
Gastroezofageálna refluxná choroba (GERD) je chronické recidivujúce ochorenie, ktoré sa prejavuje charakteristickými príznakmi a/alebo zápalovými léziami distálneho pažeráka (ezofagitída), spôsobené refluxom (retrográdnym refluxom) obsahu žalúdka a/alebo dvanástnika do pažeráka.
Slávny nemecký lekár Heinrich Quincke (Heinrich Quincke, 1842-1922) ako prvý opísal v roku 1879 gastroezofageálny reflux. Prvýkrát Winkelstein napísal o ezofagitíde spôsobenej spätným tokom obsahu žalúdka do pažeráka v roku 1935 a termín „ refluxná ezofagitída“zaviedol v roku 1946 Allison pri opise benígneho vredu pažeráka na pozadí ezofagitídy.
Prevalencia
Hlavným príznakom GERD je pálenie záhy. Podľa zahraničných výskumníkov trpí pálením záhy aspoň raz za mesiac 44 % Američanov a 7 – 10 % ho zažíva denne. Počas tehotenstva je pálenie záhy ešte častejšie (60 – 80 %).
Podľa výsledkov epidemiologických štúdií je refluxná ezofagitída zistená u 6-12% osôb, ktoré podstúpili endoskopické vyšetrenie.
Prevalencia GERD teda dosahuje 25-40 % (podľa rôznych autorov) dospelej populácie a prevyšuje prevalenciu peptického vredu a žlčových kameňov, o ktorých sa predpokladá, že postihuje až 10 % populácie.
Klasifikácia
1. Podľa endoskopického obrazu
Rozlišujte medzi endoskopicky pozitívnym a endoskopicky negatívnym GERD. Toto rozdelenie má veľký význam pri výbere taktiky liečby.
Neerozívna GERD alebo endoskopicky negatívna (s príznakmi, preukázaným refluxom, ale bez ezofagitídy) sa vyskytuje asi u 60 % pacientov.
Pri neerozívnom GERD sa častejšie pozorujú atypické prejavy (kardiálne, larygofágové, pľúcne) a ako sprievodné ochorenie je výrazne častejší syndróm dráždivého čreva.
Erozívny GERD alebo endoskopicky pozitívny (sú príznaky a preukázaná refluxná ezofagitída) sa vyskytuje približne u 40 % pacientov.
V roku 1994 bola na Svetovom gastroenterologickom kongrese v Los Angeles prijatá nasledujúca klasifikácia refluxnej ezofagitídy:
| Titul | Endoskopický obraz |
|---|---|
| A | Defekty sliznice (jeden alebo viac) s veľkosťou 5 mm alebo menej, nepresahujúce 2 záhyby sliznice pažeráka |
| IN | Slizničné defekty (jeden alebo viac) väčšie ako 5 mm, nepresahujúce 2 záhyby sliznice pažeráka |
| S | Slizničné defekty, ktoré nepresahujú 2 slizničné záhyby pažeráka, ale zaberajú menej ako 75 % obvodu pažeráka |
| D | Defekty sliznice zahŕňajúce viac ako 75 % obvodu pažeráka |
| Poznámka: | Pod pojmom "poškodenie sliznice pažeráka" sa rozumejú všetky zmeny na sliznici pažeráka, ku ktorým dochádza pri erózii, vrátane erytému (obmedzená zápalová hyperémia) a bielych fibrínových usadenín na povrchu, ulcerácie. |
2. Prítomnosťou alebo absenciou komplikácií
Rozlišujte medzi nekomplikovaným a komplikovaným GERD. Komplikácie (rovnako ako príznaky) sa zasa delia na pažerákové a extraezofageálne.
Príklady formulácie diagnózy
GERD, neerozívna forma s prevahou refluxu žlče, pretrvávajúci priebeh počas liečby PPI.
GERD: ezofagitída, stupeň B, exacerbácia (alebo remisia). Chronická laryngitída, bronchospastický syndróm.
GERD: ezofagitída, stupeň C, exacerbácia (alebo remisia). Barrettov pažerák, dysplázia vysokého stupňa.
Patogenéza
1. Znížená funkcia antirefluxnej bariéry dolného pažerákového zvierača
- Anatomické chyby - hernia pažerákového otvoru bránice, chirurgické zákroky na pažerákovom otvore bránice alebo v jej blízkosti (vagotómia, resekcia kardie žalúdka).
- Zníženie tonusu dolného pažerákového zvierača v pokoji a rozvoj jeho nedostatočnosti.
- Zvýšenie počtu epizód spontánnej relaxácie dolného pažerákového zvierača (normálne nie je viac ako 50 epizód relaxácie za deň a tieto relaxácie sú viazané na príjem potravy).
2. Znížený klírens (čistenie) pažeráka v dôsledku nedostatočného slinenia na neutralizáciu kyseliny chlorovodíkovej opustenej zo žalúdka, čím sa znižuje peristaltika pažeráka.
3. Škodlivý účinok refluxantu na sliznicu pažeráka.
4. Znížená odolnosť sliznice pažeráka na škodlivé účinky agresívnych faktorov obsahu žalúdka a dvanástnika.
5. Poruchy vyprázdňovania žalúdka(pylorospazmus pri vredovej chorobe žalúdka, stenóza pyloru, diabetická gastroparéza, anémia z nedostatku železa, dlhodobé užívanie spazmolytických liekov, nitrátov, antagonistov vápnika a pod.) Spomalenie vyprázdňovania žalúdka vedie k jeho naťahovaniu, zvýšenému tlaku v ňom a v konečnom dôsledku prispieva k vypúšťaniu obsahu žalúdka do pažeráka.
6. Zvýšený intraabdominálny tlak(obezita, príjem veľkého množstva potravy, plynatosť, tehotenstvo, ascites).
7. Infekcia Helicobacter? Túto problematiku nemožno považovať za definitívne preštudovanú. Predpokladá sa, že Helicobacter pylori (HP) sa vyskytuje v samotnom pažeráku až vtedy, keď sa v ňom rozvinie metaplázia tenkého čreva, t.j. " Barrettov pažerák(ale nie u všetkých pacientov). Zároveň u pacientov infikovaných HP je Barrettov pažerák menej častý a výskyt erozívnej ezofagitídy u pacientov s peptickým vredom po eradikačnej liečbe stúpa.
Dátum vytvorenia súboru: 05. september 2011
Úprava dokumentu: 5. septembra 2011
Autorské práva Vanyukov D.A.
Gastroezofageálna refluxná choroba (refluxná ezofagitída)
V súčasnosti by sa pod pojmom "gastroezofageálna refluxná choroba" (GERD) malo rozumieť rozvoj charakteristických symptómov a (alebo) zápalovej lézie distálneho pažeráka v dôsledku opakovaného refluxu obsahu žalúdka a (alebo) dvanástnika do pažeráka. Existujú také pojmy ako "endoskopicky pozitívna gastroezofageálna refluxná choroba" a "endoskopicky negatívna gastroezofageálna refluxná choroba". V prvom prípade vzniká refluxná ezofagitída a v druhom chýbajú endoskopické prejavy ezofagitídy. Pri endoskopicky negatívnej gastroezofageálnej refluxnej chorobe sa diagnóza stanovuje na základe typického klinického obrazu, berúc do úvahy údaje získané z iných výskumných metód (röntgenové, pH-metrické a manometrické).
Jednou z komplikácií GERD je „Barrettov pažerák“ – objavenie sa metaplastického epitelu tenkého čreva v sliznici distálneho pažeráka – potenciálne prekancerózny stav.
Prevalencia GERD medzi dospelou populáciou je až 40 %.
V západnej Európe a Spojených štátoch rozsiahle epidemiologické štúdie naznačujú, že 40 % jedincov neustále (s rôznou frekvenciou) pociťuje pálenie záhy, hlavný príznak GERD. U osôb podstupujúcich endoskopické vyšetrenie horného tráviaceho traktu je ezofagitída rôznej závažnosti zistená v 12-16% prípadov. "Barrettov pažerák" sa vyvíja u 15-20% pacientov s ezofagitídou.
Príčiny refluxnej ezofagitídy
Gastroezofageálna refluxná choroba sa v rámci tradičných koncepcií považuje za neoddeliteľnú súčasť skupiny chorôb závislých od kyseliny, pretože žalúdočná kyselina chlorovodíková je hlavným patogenetickým faktorom vo vývoji symptómov a morfologických prejavov GERD. Každá epizóda refluxu je prejavom nedostatočnosti dolného pažerákového zvierača.
Predisponujúce faktory k GERD zahŕňajú oslabenie motility žalúdka až gastroparézu, zníženie tvorby slín (Sjögrenova choroba) a porušenie cholinergnej inervácie pažeráka. Určitú úlohu vo vývoji GERD zohrávajú mikroorganizmy Helicobacter pylori, ktorých prítomnosť v sliznici srdcovej časti žalúdka nepriaznivo ovplyvňuje priebeh refluxnej ezofagitídy.
Častou príčinou GERD je diafragmatická hernia, peptický vred žalúdka a dvanástnika, funkčná dyspepsia žalúdka (vredovitá a nevredová dyspepsia). Nápoje s obsahom kofeínu, citrusové plody, alkohol, mlieko, paradajky, výrobky z nich, chren, cibuľa, cesnak, paprika a iné koreniny pomáhajú zvyšovať tvorbu kyseliny v žalúdku, dráždia jeho sliznicu a znižujú tonus dolného pažeráka zvierača.
Medzi hlavné rizikové faktory GERD patria: stres, držanie tela (predĺžené ohýbanie trupu), obezita, tehotenstvo, fajčenie, diafragmatická hernia, lieky: antagonisty vápnika, betablokátory, anticholinergiká.
Patogenéza gastroezofageálnej refluxnej choroby (refluxná ezofagitída)
Gastroezofageálny reflux sa vyvíja v dôsledku:
1) zníženie funkcie antirefluxnej bariéry, ktoré sa môže vyskytnúť rôznymi spôsobmi:
Primárny pokles tlaku v dolnom pažerákovom zvierači (LES)
Zvýšenie počtu epizód spontánnej relaxácie LES. Mechanizmy, ktorými dochádza k spontánnej (alebo prechodnej) relaxácii LES, stále nie sú úplne jasné. Úloha týchto relaxácií vo fyziologických podmienkach je jasná – uvoľnenie žalúdka z prehltnutého vzduchu. Možno to závisí od narušenia cholinergného vplyvu alebo od zvýšenia inhibičného účinku oxidu dusnatého;
Jeho úplná alebo čiastočná deštrukcia, napríklad s herniou pažerákového otvoru bránice;
2) zníženie klírensu pažeráka:
Chemické - v dôsledku zníženia neutralizačného účinku slín a hydrogénuhličitanov pažerákového hlienu
Volumetrická - v dôsledku inhibície sekundárnej peristaltiky a zníženia tónu steny hrudného pažeráka.
Uvedené porušenia zníženia klírensu pažeráka vytvárajú podmienky pre dlhodobý kontakt kyseliny chlorovodíkovej a pepsínu a niekedy aj žlčových kyselín so sliznicou pažeráka.
3) škodlivé vlastnosti refluxátu (kyselina chlorovodíková, pepsín, žlčové kyseliny);
4) neschopnosť sliznice pažeráka vydržať škodlivý účinok.
Závažnosť ochorenia bude závisieť od škodlivých vlastností refluxátu a vlastností sliznice pažeráka, ktoré spočívajú v neschopnosti odolávať tomuto škodlivému účinku. Preepiteliálna úroveň ochrany sliznice môže byť narušená v dôsledku zníženia obsahu hydrogénuhličitanov v slinách.
5) porušenie vyprázdňovania žalúdka;
6) zvýšenie intraabdominálneho tlaku.
Medzi ďalšie príčiny nedostatočnosti dolného pažerákového zvierača patrí sklerodermia, tehotenstvo, fajčenie, užívanie liekov, ktoré znižujú tonus hladkého svalstva (nitráty, blokátory vápnikových kanálov, beta-adrenergné látky, aminofylín), chirurgický zákrok a pod.
Z patofyziologického hľadiska je teda GERD ochorenie závislé od kyseliny, ktoré sa vyvíja na pozadí primárneho porušenia motorickej funkcie horného tráviaceho traktu.
Príznaky gastroezofageálnej refluxnej choroby (refluxná ezofagitída)
Charakteristické príznaky gastroezofageálnej refluxnej choroby - pálenie záhy, grganie, regurgitácia, bolestivý a sťažený prechod potravy - sú pre pacientov bolestivé, výrazne zhoršujú kvalitu života a znižujú efektívnu výkonnosť. Zvlášť výrazne je znížená kvalita života pacientov s GERD s nočnými príznakmi.
Pálenie záhy - pocit pálenia za hrudnou kosťou pozdĺž pažeráka, šíriaci sa do krku - je najcharakteristickejším príznakom, vyskytuje sa u 83 % pacientov a objavuje sa v dôsledku dlhšieho kontaktu kyslého (pH menej ako 4) obsahu žalúdka s pažerákom sliznice. Charakteristickým znakom tohto príznaku je jeho zosilnenie s chybami v strave, príjmom alkoholu, sýtených nápojov, fyzickej námahy, ohýbania a v horizontálnej polohe.
Grganie ako jeden z hlavných príznakov GERD je celkom bežné a vyskytuje sa u 52 % pacientov. Pacienti sa môžu sťažovať na grganie zjedeného jedla, kyseliny, prípadne s horkosťou a nepríjemným zápachom stagnujúceho obsahu. Tieto javy sa spravidla zintenzívňujú po jedle, užívaní sýtených nápojov.
Regurgitácia jedla, pozorovaná u niektorých pacientov s GERD, sa zvyšuje pri fyzickej námahe a pri polohe, ktorá podporuje regurgitáciu.
Spolu s pálením záhy, grganím a regurgitáciou jedla sa pacienti sťažujú na bolesť a ťažkosti s prehĺtaním, ku ktorému dochádza pri prechode potravy cez pažerák (odynofágia – bolestivé prehĺtanie, dysfágia – ťažkosti s prehĺtaním). Charakteristickým znakom týchto príznakov je ich prerušovaný charakter. Základom dysfágie je hypermotorická dyskinéza pažeráka, ktorá narúša jeho peristaltickú funkciu. Výskyt pretrvávajúcej dysfágie a súčasné zníženie pálenia záhy môže naznačovať vznik striktúry pažeráka.
Často sa vyskytujú také javy ako zvýšené slinenie - ochranná reakcia počas refluxu, nepríjemná chuť v ústach - pocit kyseliny (kovová chuť) alebo horkosť.
Jedným z najcharakteristickejších príznakov GERD je bolesť v epigastrickej oblasti, ktorá sa objavuje v projekcii xiphoidného výbežku krátko po jedle a zhoršuje sa šikmými pohybmi.
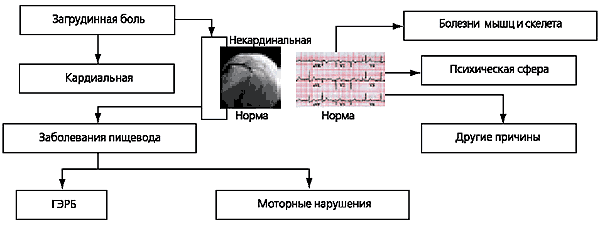
Medzi neezofageálne prejavy GERD patrí bolesť na hrudníku podobná angíne pectoris a bronchopulmonálne komplikácie.
Bolesť v hrudníku nekoronárneho pôvodu je vo väčšine prípadov spojená s patológiou pažeráka. Štúdie ukázali, že medzi pacientmi, ktorí sa sťažujú na retrosternálnu bolesť, 70 % vyšetrených nemá koronárnu patológiu a retrosternálna bolesť je spojená s ezofagospazmom alebo refluxnou ezofagitídou.
Bronchopulmonálne prejavy GERD zahŕňajú chronický kašeľ, bronchiálnu obštrukciu, pneumóniu a dysfóniu. Gastroezofageálny reflux je zistený u 30-90% pacientov s bronchiálnou astmou, čo má predispozíciu na závažnejší priebeh bronchiálnej astmy. Všeobecne uznávané dôvody rozvoja bronchiálnej obštrukcie pri GERD sú: 1) reflexný mechanizmus; 2) mikroaspirácia. Bronchopulmonálne prejavy môžu byť jediným klinickým príznakom gastroezofageálneho refluxu a spôsobiť nedostatočnú účinnosť liečby bronchiálnej astmy.
Objektívne vyšetrovacie údaje sú veľmi vzácne: zisťuje sa suchosť ústnej dutiny (xerotómia), často hypertrofované hubovité papily na jazyku v dôsledku žalúdočnej hypersekrécie, menej často symptóm ľavého alebo pravého phrenicus, vyjadrený pri laryngitíde a kombinovaný s chrapotom .
V prípade extraezofageálnych prejavov GERD vo forme chronickej bronchitídy sa v pľúcach ozývajú recidivujúce pneumónie, bronchospazmy, suché, pískavé chrapoty, vlhké stredne a jemne bublajúce chrapoty, alveolárny krepitus a predĺženie výdychu. V prítomnosti retrosternálnej bolesti nie sú žiadne poruchy frekvencie a rytmu srdcovej aktivity, keď nie je kardiovaskulárna patológia.
Komplikáciou GERD sú striktúry pažeráka, krvácanie z vredov pažeráka. Najvýznamnejšou komplikáciou GERD je "Barrettov pažerák", ktorý zahŕňa objavenie sa metaplastického epitelu tenkého čreva v sliznici pažeráka. "Barrettov pažerák" je prekancerózny stav.
Rýchlo progresívna dysfágia a strata hmotnosti môžu naznačovať rozvoj adenokarcinómu, ale tieto príznaky sa objavujú až v pokročilých štádiách ochorenia, takže klinická diagnóza rakoviny pažeráka je zvyčajne oneskorená.
Diagnóza refluxnej ezofagitídy
Medzi hlavné metódy inštrumentálnej diagnostiky patrí: endoskopické vyšetrenie, denné monitorovanie intraezofageálneho pH, RTG vyšetrenie, vyšetrenie motorickej funkcie pažeráka.
Endoskopia. U pacientov, ktorí sa sťažujú na pálenie záhy, najčastejšie endoskopické vyšetrenie odhalí príznaky refluxnej ezofagitídy rôznej závažnosti. Hyperémia a drobivosť sliznice (katarálna ezofagitída), erózia a vredy (erozívna ezofagitída rôznej závažnosti - od štádia 1 do 4 - v závislosti od oblasti lézie), prítomnosť exsudátu, fibrínu alebo príznaky krvácania odhalené. Existujú 4 štádiá ezofagitídy podľa Savaryho-Millera:
1) erytém distálneho pažeráka a oddelené nesplývajúce erózie;
2) zlúčenie, ale nie zachytenie celého povrchu sliznice erózie;
3) ulcerózna lézia dolnej tretiny pažeráka a lézia v tvare prstenca;
4) chronický vred pažeráka, stenóza, Barrettov pažerák - cylindrická metaplázia sliznice pažeráka.
Ďalej môže dôjsť k prolapsu sliznice žalúdka do pažeráka, najmä pri vracaní, skutočnému skráteniu pažeráka s umiestnením pažerákovo-žalúdočného spojenia výrazne vyššie ako bránica, refluxu obsahu žalúdka alebo dvanástnika do pažeráka. Je dosť ťažké posúdiť uzatváraciu funkciu kardie počas ezofagoskopie, pretože môže byť reflexne otvorená v reakcii na zavedenie endoskopu a insufláciu vzduchu.
V mnohých prípadoch nie sú klinické symptómy a morfologické zmeny na bunkovej úrovni sprevádzané prítomnosťou ezofagitídy (endoskopicky negatívna GERD).
Manometria. Štúdium motorickej funkcie pažeráka umožňuje študovať ukazovatele pohybu steny pažeráka a činnosť jeho zvieračov. Pri GERD manometrická štúdia odhaľuje pokles tlaku dolného pažerákového zvierača, prítomnosť hernie pažerákového otvoru bránice, zvýšenie počtu prechodných relaxácií zvierača a zníženie amplitúdy peristaltické kontrakcie steny pažeráka.
pH-metrická štúdia pažeráka. Hlavnou metódou diagnostiky GERD je pH-metria. Štúdia sa môže vykonávať ambulantne aj hospitalizovane. Pri diagnostike GERD sa výsledky pHmetrie hodnotia podľa celkového času, počas ktorého pH nadobúda hodnoty menšie ako 4 jednotky, celkového počtu refluxov za deň; počet refluxov trvajúcich viac ako 5 minút; podľa dĺžky trvania najdlhšieho refluxu.
Najvyššiu citlivosť (88-95 %) pri detekcii GERD a individuálnom výbere liekov má 24-hodinová pH-metria.
Röntgenové vyšetrenie. Röntgenové vyšetrenie pažeráka môže indikovať prítomnosť hernie pažerákového otvoru bránice, striktúru pažeráka, difúzny spazmus pažeráka a odhaliť reflux ako taký. Táto štúdia sa používa na skríningovú diagnostiku GERD.
Pri diagnostike GERD možno použiť metódy ako bilimetria, scintigrafia a Bernsteinov test. Bilimetria umožňuje overiť alkalické (žlčové) refluxy, scintigrafia odhaľuje porušenie motoricko-evakuačnej funkcie pažeráka. Tieto techniky sa používajú vo vysoko špecializovaných inštitúciách. Bernsteinov test pozostáva z infúzie 0,1 N roztoku HCl do pažeráka, čo má pri refluxnej chorobe za následok typické príznaky. Tento test môže byť užitočný pri diagnostike endoskopicky negatívneho gastroezofageálneho refluxu.
Zavedenie chromoendoskopie umožňuje odhaliť metaplastické a dysplastické zmeny v epiteli pažeráka tým, že sa na sliznicu nanesú látky, ktoré rôznym spôsobom farbia zdravé a postihnuté tkanivá.
Endoskopické ultrazvukové vyšetrenie pažeráka je hlavnou technikou, ktorá zisťuje endofyticky rastúce nádory.
Odlišná diagnóza
Bolesť na hrudníku sa môže vyskytnúť pri rôznych ochoreniach kardiovaskulárneho systému, mediastína, dýchacích orgánov, trávenia, rebier, hrudnej kosti atď. Diferenciálna diagnostika bolestí pažeráka je založená na znakoch a mechanizmoch ich vzniku, čo umožňuje ich rozlíšenie od bolesti iného pôvodu, front na angínu pectoris.
Hlavnú úlohu pri vzniku bolesti zohrávajú poruchy motility pažeráka. Dyskinéza pažeráka, najmä jeho difúzny spazmus, hypertenzia dolného pažerákového zvierača, nepropulzívne chaotické kontrakcie dolnej tretiny pažeráka, takzvaný „luskáčikový pažerák“, môžu byť sprevádzané objavením sa silnej spastickej bolesti. Podobný mechanizmus spôsobuje výskyt bolesti pri achalázii kardie: prekážka vo forme neotvárajúceho sa srdcového zvierača pozdĺž dráhy bolusu potravy spôsobuje zvýšenú kontrakciu pažeráka sprevádzanú bolesťou.
Druhým faktorom v mechanizme bolesti je gastroeyuphageal reflux (GER), pri ktorom je dôležitá peptická agresia žalúdočnej šťavy, niekedy aj obsahu dvanástnika, ak je spolu s GER aj duodenogastrický reflux. Výsledná refluxná ezofagitída môže byť sprevádzaná retrosternálnou bolesťou.
Navyše pri GER dochádza k naťahovaniu stien pažeráka, čo tiež spôsobuje bolesť. Najdôležitejšie je, že GER je často príčinou hypermotorickej dyskinézy a súvisiacej spastickej bolesti. Tento mechanizmus bolesti sa pozoruje u 60 % pacientov s gastroezofageálnou refluxnou chorobou (GERD).
Ezofagitída akejkoľvek etiológie - peptická, kandidálna, herpetická, kongestívna (v rozpore s transezofageálnym prechodom pacientov s achaláziou kardie, striktúrami, nádormi pažeráka) - môže tiež spôsobiť retrosternálnu bolesť. V závislosti od mechanizmu výskytu je povaha bolesti odlišná.
Kŕčové bolesti pri dyskinéze pažeráka majú paroxysmálny charakter. Môžu byť pálenie, tlačenie, slzenie, lokalizované za hrudnou kosťou, niekedy vyžarujúce do krku, čeľuste, chrbta, rúk, najmä vľavo, sprevádzané vegetatívnymi prejavmi (pocit tepla, potenie, chvenie v tele). Tieto bolesti sa objavujú bez jasnej súvislosti s príjmom potravy, môžu sa objaviť po jedle, v noci v kľude a pri nepokoji ich zastaví nitroglycerín, dúšok vody, prokinetika a analgetiká.
Pri GERD sa pozorujú aj iné bolesti – neprístupné, zosilnené vo vodorovnej polohe a pri predklone trupu dopredu zastavené zmenou polohy tela a užívaním antacíd.
Bolesť pažeráka môže byť konštantná, nudná alebo horiaca. Podobné bolesti na hrudníku sa pozorujú pri ezofagitíde akejkoľvek etiológie (peptická, herpetická, kandidálna), vredoch pažeráka, dlhotrvajúcej stagnácii v pažeráku pri porušení transezofageálnej pasáže u pacientov s achaláziou kardie, s nádorom alebo striktúrou pažeráka, divertikulitídou . Niekedy s ezofagitídou a pažerákovými vredmi sa bolesť vyskytuje iba pri prehĺtaní (odynofágia), závisí od povahy jedla, zvyšuje sa pri prijímaní kyslých, korenistých, veľmi horúcich alebo veľmi studených potravín.
Pri aerofágii sa pozoruje zvláštna retrosternálna bolesť kombinovaná s pocitom plnosti v epigastriu a nedostatkom vzduchu. Táto bolesť zmizne po grganí.
V klinickej praxi treba odlíšiť bolesť spôsobenú patológiou pažeráka od bolesti iného pôvodu – s infarktom myokardu, disekujúcou aneuryzmou aorty, pľúcnou embóliou, spontánnym pneumotoraxom.
Absencia známok ohrozenia života pacienta retrosternálnou bolesťou nevylučuje potrebu objasniť jej zdroj. Obzvlášť veľké ťažkosti vznikajú pri diferenciálnej diagnostike bolesti pažeráka s angínou pectoris.
Pseudokoronárna bolesť (podobná angíne) pri ochoreniach pažeráka sa pozoruje u 20-60% pacientov, čo často vedie k chybnej diagnóze. Koronarografia, vykonaná pre retrosternálnu bolesť, v 30% prípadov neodhalí zmeny na koronárnych artériách. Na druhej strane, u starších pacientov sa často kombinuje GERD a koronárna choroba srdca (ICHS). V tomto prípade môže mať bolesť koronárny a pseudokoronárny charakter.
V patológii pažeráka bolesť závisí nielen od objemu jedla, ale aj od jeho povahy (akútna, veľmi studená alebo horúca). Môžu trvať dlhšie ako záchvat angíny, prestať so zmenou polohy tela, dúškom vody, antacidá. Pri angíne pectoris možno v dôsledku viscero-viscerálnych reflexov pozorovať grganie a nevoľnosť, ako pri bolestiach pažeráka, ale pri angíne pectoris sa zaznamenáva depresívny duševný stav (strach z blížiacej sa smrti), dýchavičnosť a slabosť, čo je netypické pre ochorenia pažeráka.
Ak podľa klinických príznakov nie je možné objasniť povahu bolesti, pacient musí v prvom rade vylúčiť ochorenie koronárnych artérií. K tomu sa zisťuje prítomnosť rizikových faktorov ischemickej choroby srdca (vek, pohlavie, dedičnosť, arteriálna hypertenzia, hyperlipidémia a pod.), príznaky poškodenia kardiovaskulárneho systému (hypertrofia ľavej komory, zmeny srdcových ozvov, šelesty) sú zistené. Na diagnostiku ischemickej choroby srdca sa používajú inštrumentálne metódy: denné monitorovanie EKG, bicyklová ergometria, echokardiografia (v pokoji a pri záťaži), rádionuklidové štúdie (perfúzna scintigrafia myokardu) a ak tieto metódy nie sú informatívne, tak aj koronarografia.
Vylúčenie závažnej koronárnej patológie umožňuje dôkladnejšie vyšetrenie pažeráka.
Dostupnou a spoľahlivou metódou diferenciálnej diagnostiky, ktorá sa nedávno objavila, je rabeprazolový test - vymiznutie zodpovedajúcich symptómov (bolesť na hrudníku alebo bronchopulmonálne prejavy) do jedného dňa od začiatku užívania 20 mg rabeprazolu. Táto metóda je založená na jedinečnej schopnosti rabeprazolu, na rozdiel od iných inhibítorov protónovej pumpy, zastaviť príznaky GERD do 24 hodín.
Klasifikácia. Podľa klasifikácie v Los Angeles, schválenej Svetovou organizáciou gastroenterológie v roku 1994, ezofagitída zahŕňa len také zmeny v pažeráku, pri ktorých dochádza k poškodeniu celistvosti sliznice vo forme erózií alebo vredov. Edém, zvýšený vaskulárny vzor nedávajú dôvody na diagnózu ezofagitídy. V súlade s tým bola podľa endoskopických štúdií navrhnutá nová klasifikácia, ktorá zahŕňa inú formu ochorenia - neerozívnu refluxnú chorobu:
1. Neerozívna refluxná choroba (endoskopicky negatívna GERD).
2. Erozívna refluxná choroba (endoskopicky pozitívna GERD):
izolované erózie s priemerom menším ako 5 mm;
izolované erózie s priemerom väčším ako 5 mm;
Konfluentná erózia medzi dvoma záhybmi sliznice;
Erózie po celom obvode sliznice; 3. Komplikácie - vred, striktúra, Barrettov pažerák.
Liečba gastroezofageálnej refluxnej choroby (refluxná ezofagitída)
Liečba by mala byť zameraná na zníženie refluxu, zníženie škodlivých vlastností refluxu, zlepšenie klírensu pažeráka a ochranu sliznice pažeráka.
V súčasnosti sú hlavné princípy liečby GERD nasledovné. Pri liečbe GERD sú potrebné vysoké dávky liekov alebo ich kombinácie. Ak pacientovi nie je predpísaná udržiavacia liečba, potom je pravdepodobnosť recidívy erozívnej ezofagitídy do roka 90%. Z toho vyplýva povinná potreba udržiavacej liečby. Termíny účinnej liečby erozívnej ezofagitídy sú 8-12 týždňov. To znamená, že základný priebeh liečby by mal byť aspoň jeden mesiac a potom v priebehu 6-12 mesiacov by mal pacient dostať udržiavaciu liečbu.
Úprava životného štýlu je u väčšiny pacientov základom účinnej antirefluxnej liečby. V prvom rade je potrebné vylúčiť fajčenie a normalizovať telesnú hmotnosť, vyhnúť sa používaniu kyslých ovocných štiav, potravín, ktoré zvyšujú tvorbu plynov, ako aj tukov, čokolády, kávy, cesnaku, cibule, papriky, vylúčiť alkohol, veľmi pikantné, teplé alebo studené jedlá a sýtené nápoje.
Pacienti by sa mali vyhýbať prejedaniu a nemali by jesť pred spaním.
Vyvýšenie hlavového konca lôžka so stojanmi výrazne znižuje intenzitu refluxu. Pacientov treba upozorniť na nežiaduce užívanie liekov, ktoré znižujú tonus dolného pažerákového zvierača (teofylín, progesterón, antidepresíva, nitráty, antagonisty vápnika, enzýmové preparáty obsahujúce žlč) a samotné môžu spôsobiť zápal (nesteroidné protizápalové lieky, doxycyklín, chinidín).
Je potrebné vyhnúť sa stresu na brušné svaly, pracovať v naklonení, nosiť tesné opasky, opasky atď.
Medikamentózna liečba zahŕňa známe skupiny liekov.
1. Antacidá a algináty sú účinné pri liečbe stredne závažných a zriedkavých symptómov, najmä tých, ktoré sa vyskytujú pri porušení odporúčaní životného štýlu. Používajú sa nevstrebateľné antacidá troch generácií: 1. generácia - fosfolugel, 2. generácia - hliníkovo-horčíkové antacidá (Maalox, Melanta, Megalac, Almagel), 3. generácia - hliníkovo-horčíkové antacidá v kombinácii s kyselinou algínovou (topapkan-topaal). Algináty, vytvárajúce hustú penu na povrchu obsahu žalúdka, sa pri každej epizóde refluxu vracajú do pažeráka a poskytujú terapeutický účinok. Po prvé, vďaka obsahu antacíd majú acidoneutralizačný účinok a po druhé, keď sa dostanú do pažeráka, vytvoria ochranný film, ktorý vytvorí gradient pH medzi sliznicou a lúmenom pažeráka a chráni sliznicu z agresívneho vplyvu žalúdočnej šťavy.
Antacidá sa majú užívať často, 1-2 tablety alebo 1-2 odmerané balenia denne, zvyčajne 1,5-2 hodiny po jedle, 30-40 minút a večer v závislosti od závažnosti symptómov. Najúčinnejšie v liečbe GERD sú hliníkovo-horčíkové nevstrebateľné antacidá 2. generácie.
2. Prokinetika vedie k obnoveniu normálneho fyziologického stavu pažeráka, účinne zvyšuje tonus dolného pažerákového zvierača, zvyšuje peristaltiku pažeráka a zlepšuje klírens pažeráka. Prokinetické lieky motilium a coordinax (cisaprid, prepulsid) sú prostriedkami patogenetickej liečby GERD, normalizujúce motorickú funkciu horného tráviaceho traktu. Motilium tiež vedie k obnoveniu normálneho fyziologického stavu žalúdka, obnovuje jeho aktívnu peristaltiku a zlepšuje antroduodenálnu koordináciu.
Pri liečbe endoskopicky negatívneho GERD v prítomnosti katarálnej ezofagitídy sa motilium predpisuje v dávke 10 mg 4-krát denne, coordinax - 10 mg 2-krát denne. Používajú sa pri komplexnej terapii erozívnej ezofagitídy v spojení s inhibítormi protónovej pumpy.
Prokinetika, ako prostriedok patogenetickej liečby gastroezofageálneho refluxu, by sa preto mala používať pri liečbe stredne ťažkých symptómov na pozadí endoskopicky negatívnej GERD a katarálnej ezofagitídy ako monoterapia a ako súčasť komplexnej terapie spolu s inhibítormi protónovej pumpy.
3. V prítomnosti erozívnej ezofagitídy je potrebné predpísať inhibítory protónovej pumpy. Inhibítory protónovej pumpy veľmi účinne kontrolujú hladinu pH v dolnej tretine pažeráka. V dôsledku zníženia doby kontaktu kyseliny so sliznicou pažeráka príznaky ochorenia klesajú na intenzite a rýchlo (počas prvých 2 dní) miznú. Táto silná inhibícia produkcie kyseliny je hlavným faktorom pre hojenie erozívnych a ulceróznych lézií sliznice pažeráka u pacientov s GERD. Vymenovanie inhibítorov protónovej pumpy by malo byť liečbou voľby pri liečbe ťažkej ezofagitídy a priebeh liečby by mal trvať najmenej 8 týždňov.
Omeprazol, pariet (rabeprazol) sa používa v dávke 20 mg raz denne počas ôsmich po sebe nasledujúcich týždňov.
Absolútnou indikáciou na udržiavaciu terapiu počas 6-12 mesiacov je refluxná ezofagitída 3. a 4. stupňa podľa SavaryMillera, vznik peptických vredov, striktúr pažeráka a „Barrettovho pažeráka“.
4. Chirurgická liečba. Vzhľadom na neúčinnosť konzervatívnej liečby GERD v posledných rokoch sa používa laparoskopická Nissenova fundoplastika, ktorá poskytuje nižšiu pooperačnú mortalitu, rýchlejšiu rehabilitáciu v porovnaní s tradičnou otvorenou (transtorakálnou) fundoplastikou a dobré dlhodobé výsledky v 90 % prípadov.
Konzultácia liečby tradičnou orientálnou medicínou (akupresúra, manuálna terapia, akupunktúra, bylinná medicína, taoistická psychoterapia a iné nedrogové metódy liečby) sa uskutočňuje v centrálnej štvrti St. Petersburg (7-10 minút chôdze od stanice metra "Vladimirskaya / Dostojevskaja"), s od 9.00 do 21.00, bez obeda a dní voľna.
Už dlho je známe, že najlepší účinok pri liečbe chorôb sa dosiahne pri kombinovanom použití „západného“ a „východného“ prístupu. Výrazne skrátiť dobu liečby, znižuje pravdepodobnosť recidívy ochorenia. Keďže „východný“ prístup okrem techník zameraných na liečbu základného ochorenia venuje veľkú pozornosť „čisteniu“ krvi, lymfy, ciev, tráviaceho traktu, myšlienok a pod. – často je to dokonca nevyhnutná podmienka.
Konzultácia je bezplatná a k ničomu vás nezaväzuje. Na nej veľmi žiaduce všetky údaje o vašich laboratórnych a inštrumentálnych výskumných metódach za posledných 3-5 rokov. Po strávení iba 30-40 minút svojho času sa dozviete o alternatívnych metódach liečby, učte sa ako zlepšiť účinnosť už predpísanej terapie a čo je najdôležitejšie, o tom, ako môžete sami bojovať s chorobou. Možno budete prekvapení - ako bude všetko logicky postavené a pochopenie podstaty a príčin - prvý krok k úspešnému riešeniu problému!
Gastroezofageálna refluxná choroba (GERD) je chronické recidivujúce ochorenie charakterizované morfologickou zmenou sliznice pažeráka v dôsledku retrográdneho refluxu obsahu žalúdka alebo gastrointestinálneho traktu, ktoré sa prejavuje pažerákovými a extraezofageálnymi symptómami.
V posledných rokoch sa zvýšila frekvencia prejavov aj frekvencia detekcie tejto patológie. Ešte v roku 1999 domáci vedci citovali štatistiky o prevalencii GERD medzi deťmi v rozmedzí 2-4%. V súčasnosti nie je známa skutočná frekvencia GERD u detí, kolísanie sa pohybuje od 8,7 do 49 %. Treba tiež poznamenať trend smerom k "omladeniu" tejto patológie.
Evolúcia GERD môže viesť k rozvoju metaplastických zmien v pažeráku. Neexistujú presné údaje o prevalencii tohto stavu u detí, ale samotná skutočnosť zvýšenia frekvencie Barrettovho pažeráka u detí je tiež nepochybná. Osobitný význam pre problém GERD má vysoké riziko malignity metaplázie.
Bezprostrednou príčinou vedúcou k rozvoju GERD je gastroezofageálny reflux (GER), nedobrovoľný únik alebo reflux žalúdočného/gastrointestinálneho obsahu do pažeráka.
Aby sa zabránilo odlievaniu, existuje "antirefluxná" bariéra, ktorá reguluje takzvané "zatváracie" a "otváracie" mechanizmy. Prvé bránia refluxu, prevaha tých druhých naopak vytvára predpoklady pre jeho vznik.
V mechanizme uzatvárania kardie hrá hlavnú úlohu dolný pažerákový zvierač (LES) - ide o zhrubnutie srdcového svalu, ktoré má špeciálnu inerváciu, prekrvenie a špecifickú autonómnu motilitu.
Fyziologické fungovanie NPS je podporované:
kompresné pôsobenie membrány. K tomu dochádza v dôsledku kontrakcie pravého crus bránice a diafragmaticko-ezofageálnej fascie počas inšpirácie, zvyšuje sa tlak LES.
Dĺžka brušného pažeráka. Tento indikátor je priamo úmerný životaschopnosti antirefluxnej bariéry. Normálne je dĺžka tohto segmentu viac ako 2 cm.Treba si uvedomiť, že u novorodencov je dĺžka LES menšia ako 1 cm a približuje sa k norme do 3. mesiaca života.
Ostrý uhol His a konzistencia Gubarevovho záhybu.
Dĺžka vysokotlakovej zóny. Táto zóna sa nachádza v oblasti pažeráka a žalúdka, jej dĺžka je 1 cm u novorodencov a 2-4 cm u dospelých.
Úroveň intraabdominálneho tlaku. Ukazovatele vnútrobrušného tlaku do 6-8 cm od vodného stĺpca zabezpečujú uzavretie brušného pažeráka.
Na druhej strane sú mechanizmy otvárania kardie spojené so zvýšením vnútrobrušného tlaku (pri kašli, zápche atď.); s dyskoordináciou motility žalúdka a pažeráka vrátane peristaltických a evakuačných funkcií. Je potrebné poznamenať, že poruchy funkcie evakuácie žalúdka u novorodencov môžu priamo súvisieť s neurologickými poruchami, ako aj s dozrievaním tejto funkcie niekoľko týždňov po narodení.
V patogenéze výskytu GER je teda vedúca nerovnováha medzi „zatváracím“ a „otváracím“ mechanizmom, ku ktorej dochádza z nasledujúcich dôvodov:
Absolútna nedostatočnosť kardie (malformácie pažeráka, chirurgické zákroky na pažeráku a kardiu, dysplázia spojivového tkaniva, poškodenie CNS atď.);
Relatívna nedostatočnosť kardia (morfofunkčná nezrelosť LES u detí do 12-18 mesiacov, disproporcie v predĺžení tela a pažeráka, autonómna dysfunkcia, prechodná relaxácia LES atď.).
GER môže existovať ako fyziologický proces, pričom fyziológiu tohto javu podporujú ochranné faktory: odolnosť sliznice pažeráka, účinný klírens (t. j. schopnosť samočistenia prostredníctvom peristaltiky), tlmivý účinok slín a tzv. včasná evakuácia obsahu žalúdka.
Fyziologický proces sa môže stať patologickým pod vplyvom provokujúcich faktorov:
Porušenie režimu, kvality, objemu výživy;
Zvýšený intraabdominálny tlak (zápcha, nedostatočná fyzická aktivita, predĺžená naklonená poloha tela atď.);
Užívanie liekov, ktoré znižujú tlak LES (anticholinergiká, sedatíva, hypnotiká, b-blokátory, nitráty atď.);
Zlé návyky (fajčenie, alkohol).
Patologický GER sa realizuje vtedy, keď je narušená rovnováha medzi faktormi ochrany a faktormi agresivity. V dôsledku toho sa zvyšuje trvanie expozície refluxátu na sliznici pažeráka. Podľa domácich výskumníkov u novorodencov prevláda zásaditý reflux. V tomto prípade dochádza k poškodeniu sliznice pažeráka pod vplyvom lyzolecitínu a žlčových kyselín za účasti trypsínu. Výsledkom takejto agresie je najčastejšie výrazná fibrinózno-erozívna ezofagitída.
Kyselina chlorovodíková a aktivovaný pepsín ako faktory agresivity nadobúdajú na význame vo vyššom veku a často vedú k stenóze pažeráka.
Ukázalo sa, že prítomnosť oboch refluxantov v dutine pažeráka prispieva nielen k vzniku ezofagitídy, ale aj k črevnej metaplázii epitelu, teda Barrettovho pažeráka. Takto metaplastifikovaný epitel môže za určitých podmienok podliehať dysplázii, ktorá je základom pre vznik adenokarcinómu. Dôležitú úlohu vo vývoji metaplázie a dysplázie epitelu zohrávajú žlčové kyseliny, ktoré nielenže majú škodlivý účinok na epitel, ale prispievajú aj k malignancii. Najmä žlčové kyseliny zvyšujú aktivitu cyklooxygenázy-2 v epiteliálnych bunkách sliznice pažeráka, čím podporujú proliferačné procesy.
Podľa niektorých správ môže k výskytu GERD prispieť eradikačná terapia, ktorá znižuje peristaltickú aktivitu žalúdka pri zachovaní funkcie tvorby kyseliny.
Klinický obraz GERD je rôznorodý. Priraďte pažerákové a extraezofageálne symptómy.
Príznaky pažeráka: pálenie záhy (pocit pálenia v hrudníku); regurgitácia (pasívny únik obsahu žalúdka); grganie (dostať vzduch do ústnej dutiny, ako aj kyslý a horký obsah); bolesť v hrudi; odynofágia (bolesť alebo nepohodlie pri prechode potravy cez pažerák); dysfágia (zhoršené prehĺtanie); nevoľnosť; zvracať; príznak "mokrého vankúša" (ako prejav regurgitácie).
Extraezofageálne príznaky sa delia na otorinolaryngologické, bronchopulmonálne, kardiologické, stomatologické.
Mechanizmy rozvoja extraezofageálnych prejavov GERD sú spojené jednak s mikroaspiráciou obsahu žalúdka do orofaryngu, nosohltana, dolných dýchacích ciest, jednak s aktiváciou tzv. nociceptorov poškodenej sliznice pažeráka a priamym dráždením vagus nerv, čo vedie k reflexnému bronchospazmu alebo laryngospazmu.
Najčastejšími respiračnými prejavmi spojenými s GER sú bronchiálna astma (podľa rôznych zdrojov frekvencia tejto patológie dosahuje 80 %), chronická pneumónia, recidivujúca a chronická bronchitída, zápal stredného ucha a sínusitídy, spánkové apnoe a syndróm náhleho úmrtia.
Kardiologické prejavy GER sú charakterizované bolesťou maskujúcou sa ako angina pectoris. Takáto bolesť sa spravidla vyskytuje vo vodorovnej polohe tela. Je tiež možné vyvinúť arytmie. Kardiovaskulárne prejavy sa vyskytujú v dôsledku ezofagokardiálneho reflexu.
Medzi zubné prejavy patrí erózia zubnej skloviny a vznik kazu.
Treba poznamenať, že klinické prejavy GERD závisia od veku dieťaťa. U malých detí dominujú poruchy dýchania, regurgitácia a syndrómy zvracania. U starších detí sú zaznamenané výrazné "pažerákové" sťažnosti.
Diagnóza GERD je založená na súbore diagnostických kritérií: klinické, endoskopické, histologické, pH monitorovanie, rádiologické, manometrické, ultrazvukové atď.
Na posúdenie zápalových zmien v pažeráku sa používa klasifikácia G. Tytgata modifikovaná V. F. Privorotským et al., podľa ktorej sa rozlišujú štyri stupne ezofagitídy a tri stupne poruchy motorických funkcií.
I stupeň. Stredne výrazný fokálny erytém a (alebo) drobivosť sliznice brušného pažeráka. Stredne výrazné motorické poruchy v oblasti LES (stúpanie línie Z do 1 cm), krátkodobo provokovaný medzisúčet (pozdĺž jednej zo stien) prolaps do výšky 1-2 cm, znížený tonus LES.
II stupňa. Rovnaká + celková hyperémia brušného pažeráka s fokálnym fibrinóznym plakom a možným výskytom jednotlivých povrchových erózií, častejšie lineárnej formy, ktoré sa nachádzajú na vrcholoch záhybov sliznice pažeráka. Motorické poruchy: zreteľné endoskopické príznaky insuficiencie srdcového zvierača (NCJ), celkový alebo medzisúčet vyprovokovaný prolaps do výšky 3 cm s možnou čiastočnou fixáciou v pažeráku.
III stupňa. To isté + rozšírenie zápalu do hrudného pažeráka. Viacnásobné (niekedy splývajúce) erózie, ktoré nie sú kruhové. Je možná zvýšená kontaktná zraniteľnosť sliznice. Motorické poruchy: rovnaké + výrazný spontánny alebo provokovaný prolaps nad crura bránice s možnou čiastočnou fixáciou.
IV stupňa. Ezofageálny vred. Barrettov syndróm. Stenóza pažeráka.
Je potrebné zdôrazniť, že často v pediatrickej praxi môže byť poškodenie pažeráka pri GERD endoskopicky nerozoznateľné. V tomto ohľade sa v poslednom čase široko používajú výrazy „endoskopicky negatívny“ alebo „endoskopicky pozitívny“ GERD.
Podľa ruských vedcov teda zo 473 detí s diagnózou GERD boli klinické a endoskopické príznaky prítomné u 89 %, iba endoskopické – u 7 % a 4 % detí malo iba klinické prejavy.
Histologické vyšetrenie u detí sa vykonáva podľa nasledujúcich indikácií:
Nesúlad medzi endoskopickými a rádiologickými údajmi v nejasných prípadoch;
Atypický priebeh erozívnej a ulceróznej ezofagitídy;
Podozrenie na metaplastický proces v pažeráku;
Papilomatóza pažeráka;
Podozrenie na malignitu nádoru pažeráka.
Histologický obraz refluxnej ezofagitídy je charakterizovaný hyperpláziou epitelu vo forme zhrubnutia vrstvy bazálnych buniek a predĺžením papíl, ako aj lymfoplazmacytickou infiltráciou a množstvom ciev submukóznej vrstvy.
GER je možné zistiť dennou intragastrickou pH-metriou, počas ktorej sa zisťuje celkový počet refluxných epizód počas dňa a ich trvanie. Normálne je pH v pažeráku 5,5-7,0 a zníženie pH pod 4 sa považuje za spoľahlivé kritérium pre obdobie pozorovania GER. Pri hodnotení výsledkov pH-metrie sa používajú štandardné indikátory vyvinuté T. R. DeMeesterom (1993).
Báriová kontrastná rádiografia sa v súčasnosti menej bežne používa pri diagnostike samotného GER. Zároveň zostáva veľmi informatívnou štúdiou na identifikáciu anomálií gastrointestinálneho traktu, ktoré zhoršujú jeho motilitu. V tomto smere sa dnes kontrastná rádiografia považuje za metódu identifikácie organickej príčiny GER a riešenia otázky možnosti a účelnosti jej eliminácie vr. chirurgicky.
Ezofageálna manometria je najpresnejšou metódou na hodnotenie funkcie LES. Umožňuje registrovať tlak v rôznych častiach pažeráka, pri dýchaní a prehĺtaní, ako aj vyhodnocovať charakter peristaltických vĺn. Tlak v rozmedzí 15-30 mm Hg. čl. zodpovedá norme, pokles o menej ako 10 mm Hg. čl. indikuje hrubú patológiu LES, od 10 do 15 mm Hg. čl. - o nedostatočnosti NPS a nad 30 mm Hg. čl. o achalázii pažeráka.
Bilimetria je metóda založená na refluxnej spektrofotometrii; umožňuje 24-hodinové monitorovanie duodeno-gastroezofageálneho refluxu.
Intraezofageálna impedancemetria odhaľuje reflux, jeho výšku, trvanie a agresivitu (AR), ako aj rýchlosť a účinnosť ezofageálneho klírensu (CL). Patologický reflux je registrovaný pri AR > 10 %. Hodnota CL< 10% свидетельствует о нарушении клиренса.
Štúdia rádionuklidov - retencia izotopov v pažeráku dlhšie ako 10 minút umožňuje určiť oneskorený klírens pažeráka. Táto metóda tiež umožňuje fixáciu mikroaspirácie vyvolanej refluxom. Citlivosť kolíše v širokom rozmedzí – od 10 do 80 %.
Konzervatívna liečba GERD je založená na troch princípoch:
Diétna terapia.
posturálna terapia.
Liečebná terapia.
U malých detí sa ako diétna korekcia odporúča používať takzvané antirefluxné zmesi. Terapeutický účinok takýchto produktov je založený na zahusťovaní obsahu žalúdka, čo znižuje motorickú aktivitu žalúdka a zabraňuje refluxu do pažeráka. Ako zahusťovadlá sa používa ryžový škrob alebo guma (lepok zo svätojánskeho chleba). Pri výbere terapeutickej zmesi sa uprednostňujú aj zmesi obsahujúce kazeín. Kazeín sa v žalúdku ľahko zrazí a vytvorí hustú hrudku, ktorá prispieva k spomaleniu trávenia a zníženiu motorickej aktivity žalúdka. Antirefluxné zmesi je možné použiť pri plnom kŕmení alebo čiastočne nahradiť bežnú upravenú receptúru, ktorá je daná intenzitou regurgitácie a terapeutickým účinkom. Na trhu je pomerne široký výber antirefluxných zmesí: Enfamil AR, Frisovoy, Nutrilon AR, Samper-Lemolak.
U starších detí je princípom racionálnej stravy časté, zlomkové, mechanicky a chemicky šetriace jedlá. Znižuje sa celkové množstvo živočíšnych tukov, ktoré znižujú tonus LES (smotana, maslo, tučné ryby, bravčové, husacie, kačacie, jahňacie, cukrovinky, smotany atď.). Zároveň sa zvyšuje podiel proteínovej zložky, čím sa zvyšuje tonus LES. Ostatné dráždivé potraviny, ktoré znižujú tonus LES sú vylúčené – citrusové plody, paradajky, káva, čaj, čokoláda, mäta, cibuľa, cesnak, alkohol. Posledné jedlo by malo byť najneskôr 3 hodiny pred spaním a obsahuje ľahko stráviteľné jedlá (kvasené mlieko, zelenina, cereálie, omelety). Nápoje by sa mali konzumovať s jedlom, ale nie po jedle.
Posturálna terapia pomáha vyčistiť pažerák a znížiť reflux. Kŕmenie dieťaťa (ako cez deň, tak aj v noci!) sa vykonáva pod uhlom 45-60 stupňov. Čelo postele sa zdvihne pomocou tyčí o 10-15 cm.
Znížte hmotnosť pri obezite;
Po jedle si neľahnite;
Vyhnite sa tesnému oblečeniu, pevným pásom;
Vyhnite sa hlbokým ohybom, dlhodobému pobytu v ohnutej polohe, zdvíhaniu závažia nad 8-10 kg rukami atď .;
Vyhnite sa užívaniu množstva liekov (sedatíva, hypnotiká, trankvilizéry, antagonisty vápnika, teofylíny, anticholinergiká);
Prestaň fajčiť.
Medikamentózna liečba GERD je zameraná na obnovenie motorickej funkcie horného tráviaceho traktu, na normalizáciu funkcie žalúdka vylučujúcu kyseliny a na ochranný účinok na sliznicu pažeráka.
Na účely neutralizácie kyseliny sa používajú antacidá (Phosphalugel, Almagel, Maalox). Sú účinné pri liečbe GER bez ezofagitídy, ako aj pri refluxnej ezofagitíde I.-II.
Z prokinetiká sa úspešne používa antagonista dopamínového receptora domperidón (Motilium). Liek sa predpisuje 30-40 minút pred jedlom a v noci.
Pri liečbe refluxnej ezofagitídy stupňa II-III-IV sa odporúčajú antisekrečné lieky (blokátory H2-histamínu, inhibítory protónovej pumpy (PPI)).
Blokátory H2 receptorov sa široko používajú. Početné klinické štúdie ukázali, že k hojeniu sliznice pažeráka dochádza v 65 – 75 % prípadov počas 8-týždňovej liečby. Ranitidín (150 mg) a famotidín (20 mg) sa predpisujú jedenkrát večer po večeri (najneskôr do 20:00). Po dlhú dobu sa lieky používajú v polovičnej dennej dávke, aby sa zabránilo exacerbácii ochorenia. Antisekrečný účinok blokátora Na +, K + -ATPázy Omeprazol je lepší ako u iných liekov. Inhibíciou protónovej pumpy omeprazol poskytuje výrazné a predĺžené potlačenie sekrécie žalúdočnej kyseliny. Liečivo nemá vedľajšie účinky, pretože v aktívnej forme existuje iba v parietálnej bunke. Omeprazol sa zvyčajne predpisuje v dennej dávke 10 mg počas 3-4 týždňov. V niektorých prípadoch je potrebné predpísať malým deťom inhibítory syntézy kyseliny chlorovodíkovej: ranitidín (Zantac) a / alebo famotidín v dávke 5-10 mg / kg na dávku každých 6 hodín, s poslednou dávkou v noci.
IPP, hoci majú výrazný antisekrečný účinok, nemajú prakticky žiadny vplyv na tón LES. Ich klinický účinok je spôsobený znížením tvorby kyseliny v žalúdku, znížením agresivity refluxátu a priaznivým účinkom na žalúdok a dvanástnik.
Možný mechanizmus účinku antisekrečných liečiv na NPS je nepriamy. Akákoľvek terapia, ktorá potláča sekréciu žalúdka, vedie k zvýšeniu sekrécie gastrínu znížením inhibičného účinku kyslého obsahu žalúdka na G bunky produkujúce gastrín a gastrín pravdepodobne zvyšuje tonus LES. Tento účinok bol do značnej miery pripisovaný H2-blokátorom, ukázalo sa však, že ich účinok na tonus LES má aj iné, zatiaľ neidentifikované zložky. PPI tiež zvyšujú hladiny gastrínu v krvi najmenej u jednej tretiny pacientov 2-4 krát, ale neovplyvňujú významne motilitu pažeráka.
Vzhľadom na významnú úlohu vegetatívnych dysfunkcií pri vzniku GERD je vhodné poradiť sa s odborným psychoneurológom s následnou korekciou vegetatívneho stavu a neurologických porúch.
Ako fyzioterapeutické postupy sa u pacientov s GERD ukazuje, že vykonávajú SMT-forézu (SMT - sínusové modulované prúdy) s Cerucalom v epigastrickej oblasti, UHF (terapia s použitím decimetrového rozsahu elektromagnetického poľa) na zóne goliera a elektrospánok.
Indikácie pre chirurgickú liečbu sú:
Neúčinnosť konzervatívnej terapie, ktorá sa prejavuje vo forme ťažkých, znižujúcich kvalitu života, klinických symptómov alebo vo forme dlhotrvajúcich endoskopických príznakov refluxnej ezofagitídy III-IV stupňa na pozadí opakovaných kurzov liekovej terapie;
Komplikácie GERD (krvácanie, striktúry, Barrettov pažerák).
V súčasnosti sa používajú dva typy operácií: fundoplikácia Nisson a operácia Thal-Ashcraft a Boix-Ochoa.
GERD je teda multifaktoriálne ochorenie s rôznorodým klinickým obrazom, s možným rozvojom závažných, život ohrozujúcich komplikácií, vyžadujúcich včasnú diagnostiku a adekvátnu liečbu.
V prípade záujmu o literatúru kontaktujte redakciu.
A. A. Kovalenko
S. V. Belmer, doktor lekárskych vied, profesor
RSMU, Moskva
Catad_tema Pálenie záhy a GERD - články
Gastroezofageálna refluxná choroba: diagnostika, liečba a prevencia
A. V. Kalinin
Štátny inštitút pre postgraduálne lekárske vzdelávanie Ministerstva obrany Ruskej federácie, Moskva
ABSTRAKT
Gastroezofageálna refluxná choroba: diagnostika, liečba a prevencia
Gastroezofageálny reflux (GERD) je bežné ochorenie. Donedávna sa GERD lekárom zdalo ako neškodné ochorenie s charakteristickým príznakom - pálenie záhy. V poslednom desaťročí sa GERD nachádza v zóne zvýšenej pozornosti v dôsledku jasného trendu k zvýšeniu frekvencie ťažkej refluxnej ezofagitídy a nárastu rakoviny distálneho pažeráka na pozadí "Barrettovho pažeráka". Preukázaná súvislosť s GERD pľúcnych ochorení, najmä bronchiálnej astmy, umožňuje nový prístup k ich liečbe. Prijatie novej klasifikácie refluxnej ezofagitídy prispelo k zjednoteniu endoskopických záverov. Zavedenie dennej pH-metrie umožnilo diagnostikovať ochorenie aj v endoskopicky negatívnom štádiu. Široké využitie v klinickej praxi nových liečiv (blokátory H2-receptorov, PPI, prokinetiká) výrazne rozšírilo možnosti liečby GERD, vr. a vo svojom ťažkom priebehu. Čistý S-izomér omeprazolu, esomeprazol (Nexium), sa považuje za sľubný prostriedok na liečbu a prevenciu GERD.
V poslednom desaťročí priťahuje gastroezofageálny reflux (GERD) zvýšenú pozornosť v dôsledku nasledujúcich okolností. Vo vyspelých krajinách sveta je zreteľný trend zvyšovania incidencie GERD. Pálenie záhy, hlavný príznak GERD, sa vyskytuje u 20 – 40 % dospelých v Európe a Spojených štátoch. Hodnota GERD je určená nielen jej prevalenciou, ale aj závažnosťou priebehu. Za posledných desať rokov sa ťažká refluxná ezofagitída (RE) stala 2 až 3-krát častejšou. U 10 – 20 % pacientov s RE sa vyvinie patologický stav opísaný ako „Barrettov pažerák“ (BE) a ide o prekancerózne ochorenie. Tiež sa zistilo, že GERD zaujíma dôležité miesto v genéze mnohých ORL a pľúcnych ochorení.
V diagnostike a liečbe GERD sa dosiahol významný pokrok. Zavedenie dennej pH-metrie umožnilo diagnostikovať ochorenie aj v endoskopicky negatívnom štádiu. Široké využitie nových liekov v klinickej praxi (blokátory H2-reneptorov, inhibítory protónovej pumpy – PPI, prokinetika) výrazne rozšírilo možnosti liečby aj ťažkých foriem GERD. Boli vyvinuté jasné indikácie pre chirurgickú liečbu RE.
Praktici a samotní pacienti zároveň význam tohto ochorenia podceňujú. Pacienti sa vo väčšine prípadov obracajú na lekára so žiadosťou o lekársku pomoc neskoro a dokonca aj so závažnými príznakmi sa liečia sami. Lekári si zase zle uvedomujú túto chorobu, podceňujú jej následky a neracionálne vedú RE terapiu. Je extrémne zriedkavé diagnostikovať takú závažnú komplikáciu ako je PB.
Definícia pojmu "gastroezofageálna refluxná choroba"
Pokusy definovať pojem „gastroezofageálna refluxná choroba“ čelia značným ťažkostiam:
- u prakticky zdravých jedincov sa pozoruje reflux obsahu žalúdka do pažeráka;
- dostatočne dlhá acidifikácia distálneho pažeráka nemusí byť sprevádzaná klinickými príznakmi a morfologickými príznakmi ezofagitídy;
- často s ťažkými príznakmi GERD, nie sú žiadne zápalové zmeny v pažeráku.
Ako nezávislá nozologická jednotka bola GERD oficiálne uznaná v materiáloch o diagnostike a liečbe tohto ochorenia, prijatých v októbri 1997 na interdisciplinárnom kongrese gastroenterológov a endoskopistov v Genvale (Belgicko). Bolo navrhnuté rozlišovať medzi endoskopicky pozitívnym a endoskopicky negatívnym GERD. Posledná definícia zahŕňa tie prípady, keď pacient s prejavmi ochorenia, ktoré spĺňajú klinické kritériá pre GERD, nemá poškodenú sliznicu pažeráka. GERD teda nie je synonymom pre refluxnú ezofagitídu, pojem je širší a zahŕňa ako formy s poškodením sliznice pažeráka, tak prípady (viac ako 70 %) s typickými príznakmi GERD, pri ktorých nie sú viditeľné zmeny na pažeráku. sliznice pri endoskopickom vyšetrení .
Termín GERD používa väčšina lekárov a výskumníkov na označenie chronického recidivujúceho ochorenia spôsobeného spontánnym, pravidelne sa opakujúcim retrográdnym vstupom obsahu žalúdka a/alebo dvanástnika do pažeráka, čo vedie k poškodeniu distálneho pažeráka a/alebo objaveniu sa charakteristických symptómov. (pálenie záhy, retrosternálna bolesť, dysfágia).
Epidemiológia
Skutočná prevalencia GERD bola málo študovaná. Je to spôsobené veľkou variabilitou klinických prejavov – od epizodického pálenia záhy, pri ktorom pacienti zriedkavo navštívia lekára, až po jasné príznaky komplikovanej RE vyžadujúcej nemocničnú liečbu.
Ako už bolo uvedené, medzi dospelou populáciou Európy a Spojených štátov amerických sa pálenie záhy, hlavný príznak GERD, vyskytuje u 20 – 40 % populácie, ale iba 2 % sa liečia na RE. RE sa zistí u 6-12 % jedincov podstupujúcich endoskopické vyšetrenie.
Etiológia a patogenéza
GERD je multifaktoriálne ochorenie. Je zvykom vyčleniť niekoľko faktorov predisponujúcich k jeho rozvoju: stres; chudnutie, obezita, tehotenstvo, fajčenie, hiátová prietrž, niektoré lieky (antagonisty vápnika, anticholinergiká, B-blokátory atď.), nutričné faktory (tuk, čokoláda, káva, ovocné šťavy, alkohol, akútne jedlo).
Bezprostrednou príčinou RE je dlhodobý kontakt obsahu žalúdka (kyselina chlorovodíková, pepsín) alebo dvanástnika (žlčové kyseliny, lyzolecitín) so sliznicou pažeráka.
Existujú nasledujúce dôvody, ktoré vedú k rozvoju GERD:
- nedostatočnosť uzamykacieho mechanizmu kardia;
- reflux obsahu žalúdka a dvanástnika do pažeráka;
- znížený klírens pažeráka;
- zníženie odolnosti sliznice pažeráka.
Nedostatočnosť uzamykacieho mechanizmu kardia.
Keďže tlak v žalúdku je vyšší ako v hrudnej dutine, reflux obsahu žalúdka do pažeráka by musel byť neustálym javom. V dôsledku uzamykacieho mechanizmu kardia sa však vyskytuje zriedkavo, na krátky čas (menej ako 5 minút), a preto sa nepovažuje za patológiu. Normálne pH v pažeráku je 5,5-7,0. Ezofageálny reflux by sa mal považovať za patologický, ak celkový počet jeho epizód počas dňa presiahne 50 alebo celkový čas poklesu intraezofageálneho pH<4 в течение суток превышает 4 ч.
Medzi mechanizmy, ktoré podporujú konzistentnosť funkcie pažerákovo-žalúdočného spojenia (uzamykací mechanizmus kardie), patria:
- dolný ezofageálny zvierač (LES);
- bránicovo-pažerákové väzivo;
- hlienová "zásuvka";
- ostrý uhol His, tvoriaci Gubarevov ventil;
- intraabdominálna lokalizácia dolného pažerákového zvierača;
- kruhové svalové vlákna kardia žalúdka.
Výskyt gastroezofageálneho refluxu je výsledkom relatívnej alebo absolútnej nedostatočnosti uzamykacieho mechanizmu kardia. Výrazné zvýšenie intragastrického tlaku pri zachovanom uzamykacom mechanizme vedie k relatívnej nedostatočnosti kardia. Napríklad intenzívna kontrakcia antra žalúdka môže spôsobiť gastroezofageálny reflux aj u jedincov s normálnou funkciou dolného pažerákového zvierača. Nastáva relatívna nedostatočnosť srdcovej chlopne, podľa A.L. Grebenev a V.M. Nechaeva (1995), u 9-13% pacientov s GERD. Oveľa častejšie sa vyskytuje absolútna srdcová nedostatočnosť spojená s porušením uzamykacieho mechanizmu kardia.
Hlavná úloha v uzamykacom mechanizme je priradená stavu LES. U zdravých jedincov je tlak v tejto zóne 20,8 + 3 mm Hg. čl. U pacientov s GERD klesá na 8,9 + 2,3 mm Hg. čl.
Tón LES je pod vplyvom značného počtu exogénnych a endogénnych faktorov. Tlak v ňom klesá pod vplyvom množstva gastrointestinálnych hormónov: glukagón, somatostatín, cholecystokinín, sekretín, vazoaktívny črevný peptid, enkefalíny. Niektoré z hojne používaných liekov pôsobia aj depresívne na obturátorskú funkciu kardia (cholinergné látky, sedatíva a hypnotiká, b-blokátory, nitráty a pod.). Nakoniec tón LES znižujú niektoré potraviny: tuky, čokoláda, citrusové plody, paradajky, ako aj alkohol a tabak.
Priame poškodenie svalového tkaniva LES (chirurgické zákroky, dlhotrvajúca prítomnosť nazogastrickej sondy, bougienage pažeráka, sklerodermia) môže tiež viesť ku gastroezofageálnemu refluxu.
Ďalším dôležitým prvkom uzamykacieho mechanizmu kardia je uhol His. Predstavuje uhol prechodu jednej bočnej steny pažeráka do väčšieho zakrivenia žalúdka, kým druhej bočnej steny plynule do menšieho zakrivenia. Vzduchová bublina žalúdka a vnútrožalúdočný tlak prispievajú k tomu, že záhyby sliznice, ktoré tvoria uhol His, tesne priliehajú k pravej stene, čím bránia vymršteniu obsahu žalúdka do pažeráka (Gubarevova chlopňa ).
U pacientov s hiátovou herniou sa často pozoruje retrográdny vstup obsahu žalúdka alebo dvanástnika do pažeráka. Hernia sa nachádza u 50 % pacientov vo veku nad 50 rokov a u 63 – 84 % týchto pacientov sú príznaky RE stanovené endoskopicky.
Reflux s herniou pažerákového otvoru bránice je spôsobený niekoľkými dôvodmi:
- dystopia žalúdka do hrudnej dutiny vedie k vymiznutiu His uhla a narušeniu chlopňového mechanizmu kardie (Gubarevova chlopňa);
- prítomnosť hernie eliminuje uzamykací účinok bránicových nôh vo vzťahu ku kardii;
- lokalizácia LES v brušnej dutine implikuje vplyv na ňu pozitívnym intraabdominálnym tlakom, ktorý do značnej miery potencuje uzamykací mechanizmus kardia.
Úloha refluxu žalúdočného a duodenálneho obsahu pri GERD.
Existuje pozitívny vzťah medzi pravdepodobnosťou RE a úrovňou acidifikácie pažeráka. Štúdie na zvieratách preukázali škodlivé účinky vodíkových iónov a pepsínu, ako aj žlčových kyselín a trypsínu na ochrannú slizničnú bariéru pažeráka. Vedúcu úlohu však nemajú absolútne ukazovatele agresívnych zložiek obsahu žalúdka a dvanástnika, ktoré vstupujú do pažeráka, ale zníženie klírensu a odolnosti sliznice pažeráka.
Klírens a odolnosť sliznice pažeráka.
Pažerák je vybavený účinným mechanizmom na elimináciu posunov intraezofageálnej hladiny pH na kyslú stranu. Tento ochranný mechanizmus sa označuje ako ezofageálny klírens a je definovaný ako rýchlosť poklesu chemického stimulu z ezofageálnej dutiny. Klírens pažeráka je zabezpečený aktívnou peristaltikou orgánu, ako aj alkalizačnými vlastnosťami slín a hlienu. Pri GERD dochádza k spomaleniu klírensu pažeráka, primárne spojenému s oslabením peristaltiky pažeráka a antirefluxnej bariéry.
Odolnosť sliznice pažeráka je spôsobená preepiteliálnymi, epitelovými a postepitelovými faktormi. Poškodenie epitelu začína, keď ióny vodíka a pepsín alebo žlčové kyseliny prekonajú vodnú vrstvu obklopujúcu sliznicu, ochrannú vrstvu preepitelového hlienu a aktívnu sekréciu bikarbonátu. Bunková odolnosť voči vodíkovým iónom závisí od normálnej úrovne vnútrobunkového pH (7,3-7,4). Pri vyčerpaní tohto mechanizmu nastáva nekróza a následkom ich prudkého okyslenia dochádza k bunkovej smrti. Proti tvorbe malých povrchových ulcerácií stojí zvýšenie bunkového obratu v dôsledku zvýšenej reprodukcie bazálnych buniek sliznice pažeráka. Prekrvenie sliznice je účinný postepiteliálny obranný mechanizmus proti agresii kyselín.
Klasifikácia
Podľa Medzinárodnej klasifikácie chorôb 10. revízia sa GERD zaraďuje pod K21 a delí sa na GERD s ezofagitídou (K21.0) a bez ezofagitídy (K21.1).
Pre klasifikáciu GERD má zásadný význam závažnosť RE.
V roku 1994 bola v Los Angeles prijatá klasifikácia, ktorá rozlišovala endoskopicky pozitívne a endoskopicky negatívne štádiá GERD. Pojem "poškodenie sliznice pažeráka" nahradil pojmy "ulcerácia" a "erózia". Jednou z výhod tejto klasifikácie je jej relatívne jednoduché použitie v každodennej praxi. Pri hodnotení výsledkov endoskopického vyšetrenia sa odporúčalo použiť losangelskú klasifikáciu RE (tab. 1).
Klasifikácia v Los Angeles neposkytuje charakteristiku komplikácií RE (vredy, striktúry, metaplázia). Klasifikácia od Savary-Millera (1978) modifikovaná Carissonom a kol., je teraz viac používaná. (1996) uvedené v tabuľke 2.
Zaujímavá je nová klinická a endoskopická klasifikácia, ktorá rozdeľuje GERD do troch skupín:
- neerozívna, najčastejšia forma (60 % všetkých prípadov GERD), ktorá zahŕňa GERD bez známok ezofagitídy a katarálnej RE;
- erozívna a ulcerózna forma (34%) vrátane jej komplikácií: vred a striktúra pažeráka;
- Barrettov pažerák (6%) - metaplázia vrstevnatého dlaždicového epitelu do cylindrického epitelu v distálnom úseku v dôsledku GERD (izolácia tohto BE je spôsobená tým, že táto forma metaplázie je považovaná za prekancerózny stav).
Klinika a diagnostika
Prvou etapou diagnostiky je prieskum pacienta. Z príznakov GERD má prvoradý význam pálenie záhy, kyslé grganie, pálenie v epigastriu a za hrudnou kosťou, ktoré sa často vyskytujú po jedle, pri predklone tela alebo v noci. Druhým najčastejším prejavom tohto ochorenia je retrosternálna bolesť, ktorá vyžaruje do medzilopatkovej oblasti, krku, dolnej čeľuste, ľavej polovice hrudníka a môže imitovať angínu pectoris. Pre diferenciálnu diagnostiku genézy bolesti je dôležité, čo ju vyvoláva a zastavuje. Bolesť pažeráka je charakteristická súvislosťou s príjmom potravy, polohou tela a úľavou užívaním zásaditých minerálnych vôd a sódy.
Medzi extraezofageálne prejavy ochorenia patria pľúcne (kašeľ, dýchavičnosť, často sa vyskytujúce v polohe na chrbte), otolaryngologické (chrapľavosť, sucho v hrdle) a žalúdočné (rýchle nasýtenie, nadúvanie, nevoľnosť, vracanie) symptómy.
Röntgenovým vyšetrením pažeráka je možné zistiť prenikanie kontrastu zo žalúdka do pažeráka, odhaliť herniu pažerákového otvoru bránice, vredy, striktúry a nádory pažeráka.
Pre lepšiu detekciu gastroezofageálneho refluxu a hiátovej hernie je potrebné vykonať polypozičnú štúdiu s pacientom nakloneným dopredu s namáhaním a kašľom, ako aj ležaním na chrbte so znížením hlavového konca trupu.
Spoľahlivejšou metódou na zistenie gastroezofageálneho refluxu je denná (24-hodinová) pH-metria pažeráka, ktorá umožňuje posúdiť frekvenciu, trvanie a závažnosť refluxu, vplyv polohy tela, príjmu potravy a liekov naň. Štúdium denných zmien pH a klírensu pažeráka umožňuje identifikovať prípady refluxu pred rozvojom ezofagitídy.
V posledných rokoch sa na hodnotenie klírensu pažeráka používa scintigrafia pažeráka s rádioaktívnym izotopom technécia. Oneskorenie prijatého izotopu v pažeráku dlhšie ako 10 minút naznačuje spomalenie klírensu pažeráka.
Ezofagomanometria - meranie tlaku v pažeráku pomocou špeciálnych balónových sond - môže poskytnúť cenné informácie o poklese tlaku v oblasti LES, poruchách peristaltiky a tonusu pažeráka. Táto metóda sa však v klinickej praxi používa zriedka.
Hlavná diagnostická metóda RE je endoskopická. Pomocou endoskopie je možné získať potvrdenie o prítomnosti RE a posúdiť jej závažnosť, sledovať hojenie poškodenia sliznice pažeráka.
Biopsia pažeráka s následným histologickým vyšetrením sa robí najmä na potvrdenie prítomnosti BE s charakteristickým endoskopickým obrazom, keďže BE je možné verifikovať len histologicky.
Komplikácie refluxnej ezofagitídy
Peptické vredy pažeráka sú pozorované u 2-7% pacientov s GERD, v 15% prípadov sú vredy komplikované perforáciou, najčastejšie v mediastíne. Akútna a chronická strata krvi rôzneho stupňa sa vyskytuje takmer u všetkých pacientov s peptickým vredom pažeráka a u polovice z nich sa vyskytuje ťažké krvácanie.
Stôl 1.
Los Angeles RE klasifikácia
|
RE závažnosť |
Charakteristika zmien |
| Stupeň A | Jedna alebo viac lézií sliznice pažeráka s dĺžkou nie väčšou ako 5 mm, obmedzená na jeden záhyb sliznice |
| stupeň B | Jedna alebo viacero mukóznych lézií pažeráka dlhších ako 5 mm, ohraničených slizničnými záhybmi a lézie nepresahujú medzi dvoma záhybmi |
| stupeň C | Jedna alebo viac lézií sliznice pažeráka dlhších ako 5 mm, ohraničených záhybmi sliznice, pričom lézie siahajú medzi dva záhyby, ale pokrývajú menej než 75 % obvodu pažeráka |
| stupeň D | Poškodenie sliznice pažeráka, ktoré pokrýva 75 % alebo viac jeho obvodu |
Tabuľka 2
RE klasifikácia podľa Savary-Millera modifikovaná Carissonom a kol.
Stenóza pažeráka robí ochorenie stabilnejším: dysfágia postupuje, telesná hmotnosť klesá. Striktúry pažeráka sa vyskytujú asi u 10 % pacientov s GERD. Klinické príznaky stenózy (dysfágie) sa objavia, keď sa lúmen pažeráka zúži na 2 cm.
Závažnou komplikáciou GERD je Barrettov pažerák, ktorý prudko (30-40 krát) zvyšuje riziko rakoviny. PB sa zistí počas endoskopie u 8-20 % pacientov s GERD. Prevalencia PB vo všeobecnej populácii je oveľa nižšia a dosahuje 350 na 100 000 obyvateľov. Podľa patologických štatistík na každý známy prípad pripadá 20 nerozpoznaných prípadov. Príčinou BE je reflux obsahu žalúdka, a preto sa BE považuje za jeden z prejavov GERD.
Mechanizmus tvorby PB možno znázorniť nasledovne. Pri RE sa najskôr poškodia povrchové vrstvy epitelu, potom môže vzniknúť slizničný defekt. Poškodenie stimuluje lokálnu produkciu rastových faktorov, čo vedie k zvýšenej proliferácii a metaplázii epitelu.
Klinicky sa PB prejavuje celkovými príznakmi RE a jej komplikáciami. Pri endoskopickom vyšetrení by malo byť podozrenie na BE, keď jasne červený metaplastický epitel vo forme prstovitých výbežkov vystúpi nad líniu Z (anatomický prechod pažeráka do kardie), čím sa vytlačí svetloružový dlaždicový epitel charakteristický pre pažerák. Niekedy môžu v metaplastickej sliznici pretrvávať viaceré škvrny dlaždicového epitelu – ide o takzvaný „ostrovčekový typ“ metaplázie. Sliznica prekrývajúcich sa úsekov sa nemusí meniť alebo sa môže pozorovať ezofagitída rôznej závažnosti.
Ryža. 1
Diagnóza atypického GERD s pľúcnymi prejavmi
Endoskopicky sa rozlišujú dva typy PB:
- krátky segment PB - prevalencia metaplázie je menšia ako 3 cm;
- dlhý segment PB - prevalencia metaplázie je viac ako 3 cm.
V histologickej štúdii PB sa na mieste vrstveného dlaždicového epitelu nachádzajú prvky troch typov žliaz: niektoré sú podobné fundickému, iné srdcovému a iné črevnému. Práve s črevným epitelom pri PB je spojené vysoké riziko malígnej transformácie. V súčasnosti sa takmer všetci vedci domnievajú, že o PB je možné hovoriť len v prítomnosti črevného epitelu, ktorého markerom sú pohárikovité bunky (špecializovaný typ črevného epitelu).
Posúdenie stupňa metaplastickej epiteliálnej dysplázie pri BE a jej odlíšenie od malígnej transformácie sú náročné úlohy. Konečný úsudok o malignancii v diagnosticky náročných prípadoch možno urobiť po detekcii mutácie v tumor supresívnom géne p53.
Extraezofageálne prejavy GERD
Možno rozlíšiť nasledujúce syndrómy extraezofageálnych prejavov GERD.
1. Medzi orofaryngeálne symptómy patrí zápal nosohltanu a sublingválnej mandle, vznik erózie zubnej skloviny, kaz, paradentóza, faryngitída, pocit hrčky v hrdle.
2. Otolaryngologické príznaky sa prejavujú laryngitídou, vredmi, granulómami a polypmi hlasiviek, zápalom stredného ucha, otalgiou a nádchou.
3. Bronchopulmonálne symptómy sú charakterizované chronickou recidivujúcou bronchitídou, rozvojom bronchiektázie, aspiračnou pneumóniou, pľúcnymi abscesmi, záchvatovým spánkovým apnoe a záchvatmi záchvatovitého kašľa, ako aj bronchiálnou astmou.
4. Bolesť na hrudníku spojená s ochorením srdca, prejavujúca sa reflexnou angínou s refluxom obsahu žalúdka do pažeráka.
5. Bolesť na hrudníku nesúvisiaca s ochorením srdca (nekardiálna bolesť na hrudníku) je bežnou komplikáciou GERD, ktorá si vyžaduje adekvátnu terapiu založenú na dôkladnej diferenciálnej diagnostike so srdcovou bolesťou.
Vytvorenie spojenia medzi bronchopulmonálnymi ochoreniami a GERD má veľkú klinickú hodnotu, pretože umožňuje nový prístup k ich liečbe.
Obrázok 1 ukazuje algoritmus na diagnostiku atypického GERD s pľúcnymi prejavmi navrhnutý Americkou gastroenterologickou asociáciou. Je založená na skúšobnej liečbe PPI a ak sa dosiahne pozitívny efekt, potom sa súvislosť chronického respiračného ochorenia s GERD považuje za preukázanú. Ďalšia liečba by mala byť zameraná na zabránenie refluxu obsahu žalúdka do pažeráka a ďalšiemu vstupu refluxátu do bronchopulmonálneho systému.
Veľké ťažkosti môžu nastať pri diferenciálnej diagnostike retrosternálnej bolesti spojenej s ochorením srdca (angina pectoris, kardialgia) a inými ochoreniami, ktoré spôsobujú retrosternálnu bolesť. Algoritmus diferenciálnej diagnostiky je znázornený na obrázku 2. 24-hodinové monitorovanie pH pažeráka môže pomôcť pri rozpoznaní retrosternálnej bolesti spojenej s GERD (obrázok 3).
Liečba
Cieľom liečby GERD je odstránenie ťažkostí, zlepšenie kvality života, boj proti refluxu, liečba ezofagitídy, prevencia alebo eliminácia komplikácií. Liečba GERD je častejšie konzervatívna ako chirurgická.
Konzervatívna liečba zahŕňa:
- odporúčania na dodržiavanie určitého životného štýlu a stravovania;
- medikamentózna terapia: antacidá, antisekrečné lieky (blokátory H2-receptorov a inhibítory protónovej pumpy), prokinetiká.
Boli vyvinuté nasledujúce základné pravidlá, ktoré musí pacient neustále dodržiavať bez ohľadu na závažnosť RE:
- po jedle sa vyhnite predklonu a neľahnite si;
- spať so zdvihnutým čelom postele;
- nenoste tesné oblečenie a tesné pásy, korzety, obväzy, čo vedie k zvýšeniu intraabdominálneho tlaku;
- vyhnúť sa veľkým jedlám; nejedzte v noci; obmedziť konzumáciu potravín, ktoré spôsobujú zníženie tlaku LES a majú dráždivý účinok (tuky, alkohol, káva, čokoláda, citrusové plody);
- Prestaň fajčiť;
- znížiť telesnú hmotnosť pri obezite;
- vyhnúť sa užívaniu liekov, ktoré spôsobujú reflux (anticholinergiká, spazmolytiká, sedatíva, trankvilizéry, inhibítory vápnikových kanálov, p-blokátory, teofylín, prostaglandíny, nitráty).
Antacidá.
Cieľom antacidovej terapie je znížiť kyslo-proteolytickú agresiu žalúdočnej šťavy. Zvýšením hladiny intragastrického pH tieto lieky eliminujú patogénny účinok kyseliny chlorovodíkovej a pepsínu na sliznicu pažeráka. Arzenál moderných antacíd dosiahol pôsobivú veľkosť. V súčasnosti sa vyrábajú spravidla vo forme komplexných prípravkov na báze hydroxidu hlinitého, hydroxidu horečnatého alebo hydrogénuhličitanu horečnatého, ktoré sa nevstrebávajú v gastrointestinálnom trakte. Antacidá sa predpisujú 3-krát denne 40-60 minút po jedle, kedy sa najčastejšie vyskytuje pálenie záhy a v noci. Odporúča sa dodržiavať nasledujúce pravidlo: každý záchvat bolesti a pálenia záhy by sa mal zastaviť, pretože tieto príznaky naznačujú progresívne poškodenie sliznice pažeráka.
Antisekrečné lieky.
Antisekrečná liečba GERD sa vykonáva na zníženie škodlivého účinku kyslého obsahu žalúdka na sliznicu pažeráka pri gastroezofageálnom refluxe. Blokátory H2-receptorov (ranitidín, famotidín) našli široké uplatnenie v EC. Pri použití týchto liekov sa výrazne znižuje agresivita vyhodeného obsahu žalúdka, čo prispieva k úľave od zápalového a erozívno-ulcerózneho procesu v sliznici pažeráka. Ranitidín sa predpisuje raz v noci v dennej dávke 300 mg alebo 150 mg 2-krát denne; famotidín sa používa raz v dávke 40 mg alebo 20 mg 2-krát denne.
Ryža. 2.
Diferenciálna diagnostika retrosternálnej bolesti
Ryža. 3.
Epizódy recidivujúcej bolesti na hrudníku korelujú s epizódami refluxu s pH<4 (В. Д. Пасечников, 2000).

V posledných rokoch sa objavili zásadne nové antisekrečné lieky - inhibítory H +, K + -ATPázy(PPI - omeprazol, lansoprazol, rabeprazol, esomeprazol). Inhibíciou protónovej pumpy poskytujú výrazné a predĺžené potlačenie sekrécie žalúdočnej kyseliny. PPI sú obzvlášť účinné pri peptickej erozívno-ulceróznej ezofagitíde, poskytujú hojenie postihnutých oblastí v 90-96% prípadov po 6-8 týždňoch liečby.
Najširšie uplatnenie si u nás našiel omeprazol. Z hľadiska antisekrečného účinku je tento liek lepší ako blokátory H2 receptorov. Dávkovanie omeprazolu: 20 mg 2-krát denne alebo 40 mg večer.
V posledných rokoch sa v klinickej praxi široko používajú nové PPI, rabeprazol a esomeprazol (Nexium).
Rabeprazol sa premieňa rýchlejšie ako iné PPI na aktívnu (sulfanilamidovú) formu. Z tohto dôvodu už v prvý deň užívania rabeprazolu klesá alebo úplne zmizne taký klinický prejav GERD, ako je pálenie záhy.
Značný záujem je o nový PPI - esomeprazol (Nexium), ktorý je produktom špeciálnej technológie. Ako je známe, stereoizoméry (látky, ktorých molekuly majú rovnakú sekvenciu chemických väzieb atómov, ale rozdielne usporiadanie týchto atómov voči sebe navzájom v priestore) sa môžu líšiť v biologickej aktivite. Páry optických izomérov, ktoré sú vzájomnými zrkadlovými obrazmi, sú označené ako R (z latinského rectus - rovný alebo rota dexterior - pravé koleso, v smere hodinových ručičiek) a S (sinister - vľavo alebo proti smeru hodinových ručičiek).
Esomeprazol (Nexium) je S-izomér omeprazolu av súčasnosti je prvým a jediným PPI, ktorý je čistým optickým izomérom. Je známe, že S-izoméry iných PPI sú vo farmakokinetických parametroch lepšie ako ich R-izoméry a teda racemické zmesi, ktoré sú v súčasnosti existujúcimi liekmi v tejto skupine (omeprazol, lansoprazol, pantoprazol, rabeprazol). Doteraz bol stabilný S-izomér schopný vytvoriť iba omeprazol. Štúdie na zdravých dobrovoľníkoch ukázali, že ezomeprazol je opticky stabilný v akejkoľvek dávkovej forme – na perorálne aj intravenózne použitie.
Klírens ezomeprazolu je nižší ako klírens omeprazolu a R-izoméru. Dôsledkom toho je vyššia biologická dostupnosť ezomeprazolu v porovnaní s omeprazolom. Inými slovami, veľká časť každej dávky ezomeprazolu zostáva v krvnom obehu po prvom prechode metabolizmom. Množstvo liečiva, ktoré inhibuje protónovú pumpu parietálnej bunky žalúdka, sa teda zvyšuje.
Antisekrečný účinok ezomeprazolu je závislý od dávky, zvyšuje sa počas prvých dní podávania [11]. Účinok ezomeprazolu nastáva 1 hodinu po perorálnom podaní v dávke 20 alebo 40 mg. Pri dennom podávaní lieku počas 5 dní v dávke 20 mg 1-krát denne sa priemerná maximálna koncentrácia kyseliny po stimulácii pentagastrínom zníži o 90 % (meranie sa uskutočnilo 6-7 hodín po poslednej dávke lieku ). U pacientov so symptomatickou GERD hladina intragastrického pH počas denného monitorovania po 5 dňoch užívania ezomeprazolu v dávkach 20 a 40 mg zostala nad 4 v priemere 13 a 17 hodín, v uvedenom poradí. U pacientov užívajúcich ezomeprazol 20 mg denne sa udržanie hladiny pH nad 4 počas 8, 12 a 16 hodín dosiahlo v 76 %, 54 % a 24 % prípadov. Pre 40 mg ezomeprazolu bol tento pomer 97 %, 92 % a 56 %, v uvedenom poradí (p<0,0001) .
Dôležitou zložkou, ktorá zabezpečuje vysokú stabilitu antisekrečného účinku ezomeprazolu, je jeho mimoriadne predvídateľný metabolizmus. Esomeprazol poskytuje 2-krát väčšiu stabilitu takého indikátora, ako je individuálna variabilita v supresii žalúdočnej sekrécie stimulovanej pentagastrínom, ako omeprazol v ekvivalentnej dávke.
Účinnosť ezomeprazolu pri GERD sa skúmala v niekoľkých randomizovaných, dvojito zaslepených, multicentrických štúdiách. V dvoch veľkých štúdiách zahŕňajúcich viac ako 4 000 pacientov s GERD neinfikovaných H. pylori bol ezomeprazol v denných dávkach 20 alebo 40 mg významne účinnejší pri hojení erozívnej ezofagitídy ako omeprazol v dávke 20 mg. V oboch štúdiách bol ezomeprazol významne lepší ako omeprazol po 4 aj 8 týždňoch liečby.
Úplné zmiernenie pálenia záhy (neprítomnosť počas 7 po sebe nasledujúcich dní) v skupine 1960 pacientov s GERD sa tiež dosiahlo s esomeprazolom 40 mg/deň u väčšieho počtu pacientov ako s omeprazolom, ako v deň 1 dávkovania (30 % oproti 22 %, R<0,001), так и к 28 дню (74% против 67%, р <0,001) . Аналогичные результаты были получены и в другом, большем по объему (п = 2425) исследовании (р <0,005) . В обоих исследованиях было показано преимущество эзомепразола над омепразолом (в эквивалентных дозах) как по среднему числу дней до наступления полного купирования изжоги, так и по суммарному проценту дней и ночей без изжоги в течение всего периода лечения. Еще в одном исследовании, включавшем 4736 больных эрозивным эзофагитом, эзомепразол в дозе 40 мг/сут достоверно превосходил омепразол в дозе 20 мг/сут по проценту ночей без изжоги (88,1%, доверительный интервал - 87,9-89,0; против 85,1%, доверительный интервал 84,2-85,9; р <0,0001) .Таким образом, наряду с известными клиническими показателями эффективности лечения ГЭРБ, указанные дополнительные критерии позволяют заключить, что эзомепразол объективно превосходит омепразол при лечении ГЭРБ. Столь высокая клиническая эффективность эзомепразола существенно повышает и его затратную эффективность. Так, например, среднее число дней до полного купирования изжоги при использовании эзомепразола в дозе 40 мг/сут составляло 5 дней, а оме-празола в дозе 20 мг/сут - 9 дней . При этом важно отметить, что омепразол в течение многих лет являлся золотым стандартом в лечении ГЭРБ, превосходя по клиническим критериям эффективности все другие ИПП, о чем свидетельствует анализ результатов более чем 150 сравнительных исследований .
Esomeprazol bol tiež študovaný ako udržiavací liek pri GERD. Dve dvojito zaslepené, placebom kontrolované štúdie zahŕňajúce viac ako 300 pacientov s GERD s vyliečenou ezofagitídou hodnotili tri dávky ezomeprazolu (10, 20 a 40 mg/deň) podávané počas 6 mesiacov.
Pri všetkých študovaných dávkach bol ezomeprazol výrazne lepší ako placebo, ale zistilo sa, že najlepší pomer dávka/účinnosť pre udržiavaciu liečbu je 20 mg/deň. Sú publikované údaje o účinnosti udržiavacej dávky ezomeprazolu 40 mg/deň podávanej 808 pacientom s GERD: remisia po 6 a 12 mesiacoch bola zachovaná u 93 % a 89,4 % pacientov.
Jedinečné vlastnosti ezomeprazolu umožnili úplne nový prístup k dlhodobej liečbe GERD – terapiu na požiadanie, ktorej účinnosť bola skúmaná v dvoch 6-mesačných zaslepených, placebom kontrolovaných štúdiách, do ktorých bolo zaradených 721 a 342 pacientov s GERD, resp. Esomeprazol sa používal v dávkach 40 mg a 20 mg. V prípade nástupu symptómov ochorenia bolo pacientom dovolené užívať maximálne jednu dávku (tabletu) denne a ak symptómy neustávali, potom im bolo dovolené užívať antacidá. Pri zhrnutí sa ukázalo, že v priemere pacienti užili ezomeprazol (bez ohľadu na dávku) 1-krát za 3 dni, pričom nedostatočnú kontrolu symptómov (pálenie záhy) zaznamenalo len 9 % pacientov, ktorí dostali 40 mg ezomeprazolu, 5 % - 20 mg a 36 % - placebo (str<0,0001). Число больных, вынужденных дополнительно принимать антациды, оказалось в группе плацебо в 2 раза большим, чем в пациентов, получавших любую из дозировок эзомепразола .
Klinické štúdie teda presvedčivo naznačujú, že ezomeprazol je sľubnou liečbou GERD, a to ako v jej najťažších formách (erozívna ezofagitída), tak aj pri neerozívnej refluxnej chorobe.
Prokinetika.
Zástupcovia tejto skupiny liečivých látok majú antirefluxný účinok a tiež zvyšujú uvoľňovanie acetylcholínu v gastrointestinálnom trakte, čím stimulujú motilitu žalúdka, tenkého čreva a pažeráka. Zvyšujú tonus LES, urýchľujú evakuáciu zo žalúdka, majú pozitívny vplyv na klírens pažeráka a znižujú gastroezofageálny reflux.
Domperidón, ktorý je periférnym antagonistom dopamínového receptora, sa bežne používa ako prokinetikum pri EC. Domperidón sa predpisuje 10 mg (1 tableta) 3-krát denne 15-20 minút pred jedlom.
Pri EC spôsobenej refluxom obsahu dvanástnika (predovšetkým žlčových kyselín) do pažeráka, ktorý sa zvyčajne pozoruje pri cholelitiáze, sa dobrý účinok dosiahne pri užívaní netoxickej ursode-oxycholovej žlčovej kyseliny v dávke 5 mg/kg denne napr. 6-8 mesiacov.
Výber taktiky liečby.
Pri výbere liečby GERD v štádiu erozívno-ulceróznej RE treba pamätať na to, že v týchto prípadoch nie je terapia jednoduchou úlohou. K hojeniu defektu sliznice dochádza v priemere:
- 3-4 týždne pre dvanástnikový vred;
- počas 4-6 týždňov so žalúdočným vredom;
- počas 8-12 týždňov s erozívnymi a ulceróznymi léziami pažeráka.
V súčasnosti bola vyvinutá postupná schéma liečby v závislosti od závažnosti RE. Podľa tejto schémy sa odporúča začať liečbu plnou dávkou PPI už v EC stupni 0 a I, aj keď je povolené aj použitie H2-blokátorov v kombinácii s prokinetikami (obr. 4).
Liečebný režim pre pacientov s ťažkou EK (štádium II-III) je znázornený na obrázku 5. Zvláštnosťou tohto režimu sú dlhšie liečebné cykly a predpisovanie (ak je to potrebné) vysokých dávok PPI. Pri absencii účinku konzervatívnej liečby u pacientov tejto kategórie je často potrebné nastoliť otázku antirefluxnej chirurgie. O vhodnosti chirurgickej liečby by sa malo diskutovať aj v prípade komplikácií RE, ktoré nie sú prístupné medikamentóznej terapii.
Chirurgia.
Cieľom operácií zameraných na odstránenie refluxu je obnovenie normálnej funkcie kardia.
Indikácie pre chirurgickú liečbu: 1) zlyhanie konzervatívnej liečby; 2) komplikácie GERD (striktúry, opakované krvácanie); 3) častá aspiračná pneumónia; 4) PB (kvôli nebezpečenstvu malignity). Obzvlášť často sa indikácie na operáciu vyskytujú, keď sa GERD kombinuje s herniou pažerákového otvoru bránice.
Hlavným typom operácie refluxnej ezofagitídy je Nissenova fundoplikácia. V súčasnosti sa vyvíjajú a implementujú metódy fundoplikácie vykonávané prostredníctvom laparoskopu. Výhodou laparoskopickej fundoplikácie je výrazne nižšia pooperačná mortalita a rýchla rehabilitácia pacientov.
V súčasnosti sa pri PB na ovplyvnenie ložísk neúplnej intestinálnej metaplázie a ťažkej epitelovej dysplázie používajú nasledujúce endoskopické techniky:
- laserová deštrukcia, koagulácia argónovou plazmou;
- multipolárna elektrokoagulácia;
- fotodynamická deštrukcia (fotosenzibilizačné lieky sa podávajú 48-72 hodín pred zákrokom, potom sa ošetria laserom);
- endoskopická lokálna resekcia sliznice pažeráka.
Všetky vyššie uvedené metódy ovplyvňovania ložísk metaplázie sa používajú na pozadí použitia PPI, ktoré potláčajú sekréciu a prokinetiky, ktoré znižujú gastroezofageálny reflux.
Prevencia a lekárske vyšetrenie
Pre rozšírený výskyt GERD, ktorý vedie k zníženiu kvality života a riziko komplikácií pri ťažkých formách RE, je prevencia tohto ochorenia veľmi naliehavou úlohou.
Cieľom primárnej prevencie GERD je zabrániť rozvoju ochorenia. Primárna prevencia zahŕňa nasledujúce odporúčania:
- udržiavanie zdravého životného štýlu (prestať fajčiť a piť silné alkoholické nápoje);
- racionálna výživa (vyhnite sa veľkým jedlám, nejedzte v noci, obmedzte konzumáciu veľmi korenistých a teplých jedál;
- strata hmotnosti pri obezite;
- len podľa prísnych indikácií užívať lieky spôsobujúce reflux (anticholinergiká, spazmolytiká, sedatíva, trankvilizéry, inhibítory kalciových kanálov, b-blokátory, prostaglandíny, nitráty) a poškodzujúce sliznicu (nesteroidné antiflogistiká).
Ryža. 4.
Voľba liečby u pacientov s endoskopicky negatívnym alebo miernym (0-1) stupňom refluxnej ezofagitídy

Ryža. 5.
Voľba liečby pre pacientov so závažnými (II-III) stupňami refluxnej ezofagitídy

Cieľom sekundárnej prevencie GERD je znížiť frekvenciu relapsov a zabrániť progresii ochorenia. Povinnou súčasťou sekundárnej prevencie je dodržiavanie vyššie uvedených odporúčaní pre primárnu prevenciu. Sekundárna drogová prevencia do značnej miery závisí od závažnosti RE.
"Terapia na požiadanie" sa používa na prevenciu exacerbácií v neprítomnosti ezofagitídy alebo miernej ezofagitídy (RE 0-1 stupeň). Každý záchvat bolesti a pálenia záhy by sa mal zastaviť, pretože ide o signál patologického prekyslenia pažeráka, čo prispieva k postupnému poškodzovaniu jeho sliznice. Ťažká ezofagitída (najmä EC III-IV stupeň) si vyžaduje dlhodobú, niekedy trvalú udržiavaciu liečbu PPI alebo blokátormi H 2 receptorov v kombinácii s prokinetikami.
Za kritériá úspešnej sekundárnej prevencie sa považuje zníženie počtu exacerbácií ochorenia, absencia progresie, zníženie závažnosti RE a prevencia komplikácií.
Pacienti s GERD v prítomnosti endoskopických príznakov RE potrebujú dispenzárne pozorovanie s endoskopickou kontrolou aspoň raz za 2-3 roky.
Osobitná skupina by mala byť pridelená pacientom s diagnózou PB. Endoskopickú kontrolu s cielenou biopsiou sliznice pažeráka z oblasti zrakovo zmeneného epitelu je žiaduce vykonávať ročne (minimálne však raz ročne), ak v predchádzajúcej štúdii nebola dysplázia. Keď sa zistí druhý, endoskopická kontrola by sa mala vykonávať častejšie, aby sa nepremeškal moment malignity. Prítomnosť dysplázie nízkeho stupňa pri BE vyžaduje endoskopiu s biopsiou každých 6 mesiacov a ťažkú dyspláziu po 3 mesiacoch. U pacientov s potvrdenou ťažkou dyspláziou sa má zvážiť chirurgická liečba.
LITERATÚRA
1. Dean BB, CrawleyJA, SchmittCM, Wong], Of man 11. Bremeno choroby gastroezofageálneho refluxu: vplyv na produktivitu práce. Aliment Pharmacol Ther 2003 máj 15;17:1309-17.
2. DentJ, Jones R, Kahrilas P, Talley N1. Manažment gastroezofageálnej refluxnej choroby vo všeobecnej praxi. BMJ 2001;322:344-7.
3. GalmicheJP, LetessierE, Scarpignato C. Liečba gastroezofageálneho refluxu u dospelých. BMJ 199S;316:1720-3.
4. Kahrilas P.I. Gastroezofageálna refluxná choroba. JAMA 1996:276:933-3.
5. Salvatore S, Vandenplas Y. Gastroezofageálna refluxná choroba a poruchy motility. Best Pract Res Clin Gastroenterol 2003:17:163-79.
6. Stanghellini V. Manažment gastroezofageálnej refluxnej choroby. Drugs Today (Bare) 2003;39 (suppl. A):15-20.
7. Arimori K, Yasuda K, Katsuki H, Nakano M. Farmakokinetické rozdiely medzi enantiomérmi lansoprazolu u potkanov. J Pharm Pharmacol 1998:50:1241-5.
8 Tanaka M, Ohkubo T, Otani K, a kol. Stereoselektívna farmakokinetika pantoprazolu, inhibítora protónovej pumpy, u extenzívnych a slabých metabolizátorov S-mefenytoínu. Clin Pharmacol Ther 2001:69:108-13.
9. Abelo A, Andersson TV, Bredberg U, a kol. Stereoselektívny metabolizmus substituovaného benzimidazolu ľudskými pečeňovými enzýmami CYP. Drug Metab Dispos 2000:28:58-64.
10. Hassan-Alin M, Andersson T, Bredberg E, Rohss K. Farmakokinetika ezomeprazolu po perorálnom podaní
a intravenózne podávanie jednotlivých a opakovaných dávok zdravým subjektom. Eur 1 Clin Pharmacol 2000:56:665-70.
11. Andersson T, Bredberg E, Hassan-Alin M. Farmakokinetika a farmakodynamika ezomeprazolu, S-izoméru omeprazolu. Aliment Pharmacol Ther 2001:15:1563-9.
12. Lind T, Rydberg L, Kyleback A, a kol. Esomeprazol poskytuje zlepšenú kontrolu kyseliny vs. omeprazol u pacientov s príznakmi gastroezopageálneho refluxu. Aliment Pharmacol Ther 2000:14:861-7.
13. Andersson T, Rohss K, Hassan-Alin M. Farmakokinetika (PK) a vzťah medzi dávkou a odozvou ezomeprazolu (E). Gastroenterology 2000:118(doplnok 2):A1210.
14. Kahrilas PI, Falk GW, Johnson DA, a kol. Esomeprazol zlepšuje hojenie a zmiernenie symptómov v porovnaní s omeprazolom u pacientov s refluxnou ezofagitídou: randomizovaná kontrolovaná štúdia. Výskumníci štúdie Esomeprazole. Aliment Pharmacol Ther 2000:14:1249-58.
15. RichterJE, Kahrilas PJ, JohansonJ, et al. Účinnosť a bezpečnosť ezomeprazolu v porovnaní s omeprazolom u pacientov s GERD s erozívnou ezofagitídou: randomizovaná kontrolovaná štúdia. Am 1 Gastroenterol 2001:96:656-65.
16. Vakil NB, Katz PO, Hwang C, a kol. Nočné pálenie záhy je zriedkavé u pacientov s erozívnou ezofagitídou liečených ezomeprazolom. Gastroenterológia 2001:120:abstrakt 2250.
17. Kromer W, Horbach S, Luhmann R. Relatívne účinnosti inhibítorov žalúdočnej protónovej pumpy: ich
klinickom a farmakologickom základe. Pharmacology 1999: 59: 57-77.
18. Johnson DA, Benjamin SB, Vakil NB a kol. Esomeprazol raz denne počas 6 mesiacov je účinnou terapiou na udržanie vyliečenej erozívnej ezofagitídy a na kontrolu symptómov gastroezofageálneho refluxu: randomizovaná, dvojito zaslepená, placebom kontrolovaná štúdia účinnosti a bezpečnosti. Am 1 Gastroenterol 2001:96:27-34.
19. Vakil NB, Shaker R, Johnson DA, a kol. Nový inhibítor protónovej pumpy esomeprazol je účinný ako udržiavacia liečba u pacientov s GERD s vyliečenou erozívnou ezofagitídou: 6-mesačná, randomizovaná, dvojito zaslepená, placebom kontrolovaná štúdia účinnosti a bezpečnosti. Aliment Pharmacol Ther 2001:15:927-35.
20. Maton PN, Vakil NB, Levine JG, a kol. Bezpečné zistenie účinnosti dlhodobej liečby ezomeprazolom u pacientov s vyliečenou erozívnou ezofagitídou. Drug Saf 2001:24:625-35.
21. Talley N1, Venables TL, Green JBR. Esomeprazol 40 mg a 20 mg je účinný v lomg-tenn manažmente pacientov s endoskopicky negatívnou GERD: placebom kontrolovaná štúdia terapie na požiadanie počas 6 mesiacov. Gastroenterology 2000:118:A658.
22. Talley N1, Lauritsen K, Tunturi-Hihnala H, a kol. Esomeprazol 20 mg udržuje kontrolu symptómov pri endoskopicky negatívnom gastroezofageálnom refluxnom ochorení: kontrolovaná štúdia s liečbou "on-demand" počas 6 mesiacov. Aliment Pharmacol Ther 2001:15:347-54.
Prednáška prezentuje moderné údaje o epidemiológii, etiológii, patogenéze gastroezofageálnej refluxnej choroby. Zvažujú sa klinické prejavy ochorenia a diferenciálna diagnostika hlavných symptómov. Načrtnutá je problematika diagnostiky a liečby gastroezofageálnej refluxnej choroby v súlade s klinickými odporúčaniami.
Gastroezofageálna refluxná choroba v praxi lekára primárnej zdravotnej starostlivosti
V prednáške sú prezentované moderné poznatky o epidemiológii, etiológii a patogenéze gastroezofageálnej refluxnej choroby. Sú opísané klinické prejavy a diferenciálna diagnostika hlavných symptómov. Otázky diagnostiky a liečby gastroezofageálnej refluxnej choroby sú uvedené z dôvodu klinických odporúčaní.
Napriek výdobytkom modernej gastroenterológie problémy diagnostiky, liečby a prevencie chorôb závislých od kyseliny, medzi ktoré patrí aj gastroezofageálna refluxná choroba (GERD), stále priťahujú pozornosť lekárov. Pacienti s acid-dependentnými ochoreniami tvoria značnú časť pacientov u lekára prvého kontaktu a diagnostika a diferenciálna diagnostika týchto stavov je častou úlohou v praxi terapeuta aj praktického lekára.
Význam GERD je daný nielen jej rastúcou prevalenciou, ale aj zhoršením priebehu: nárastom počtu komplikovaných foriem (vredy, striktúry pažeráka), rozvojom Barrettovho pažeráka ako prekancerózneho stavu, extraezofageálnym Údaje z epidemiologických štúdií naznačujú, že prevalencia GERD je vysoká, v krajinách západnej Európy dosahuje 40-50 %. Pálenie záhy, hlavný príznak GERD, sa vyskytuje u 20-40% populácie v rozvinutých krajinách a v Spojených štátoch sa pozoruje u 25 miliónov ľudí. Pri výraznom náraste počtu pacientov trpiacich GERD, viac ako polovici pacientov je diagnostikovaná jeho endoskopicky negatívna forma, dochádza k výraznému zhoršeniu kvality života. Závažnosť pálenia záhy nekoreluje so závažnosťou ezofagitídy. Podľa A.V. Kalinin, u pacientov, ktorí sa sťažovali na pálenie záhy, sa počas endoskopie zistí erozívna ezofagitída iba v 7-10% prípadov. Podľa ruských štúdií bol výskyt GERD (prítomnosť pálenia záhy a/alebo kyslej eruktácie raz týždenne a častejšie počas posledných 12 mesiacov) 23,6 %. Je potrebné poznamenať, že časté pálenie záhy (raz týždenne alebo viac) je nezávislým rizikovým faktorom pre vznik adenokarcinómu pažeráka a pri trvaní ochorenia 20 a viac rokov sa riziko vzniku rakoviny pažeráka zvyšuje 44-krát.
Definícia GERD naznačuje, že ide o ochorenie charakterizované rozvojom zápalových zmien na sliznici distálneho pažeráka a/alebo charakteristickými klinickými príznakmi v dôsledku opakovaného refluxu obsahu žalúdka/alebo dvanástnika do pažeráka. Moderný koncept GERD bola prijatá v roku 2006, keď bola zverejnená Montrealská správa o definícii a klasifikácii. gastroezofageálnyrefluxchoroba" .
Etiológia a patogenéza. V patogenéze GERD vedie, podobne ako pri iných acid-dependentných patológiách, nerovnováha medzi faktormi agresivity a ochrany sliznice pažeráka v smere prvého. Pri manažovaní pacientov treba brať do úvahy, že v prevažnej väčšine prípadov je hlavným faktorom (93 %) faktor nadmerného okyslenia pažeráka a reflux žlče tvorí len 7 %. Vo všeobecnosti sú mechanizmami vzniku GERD hypotenzia dolného pažerákového zvierača (LES), prítomnosť hernie pažerákového otvoru bránice, ktorá vedie k anatomickému zlyhaniu LES, škodlivý účinok refluxu, spomalenie dole klírens pažeráka objemový (porušenie sekundárnej peristaltiky pažeráka, ktorá zabezpečuje uvoľnenie pažeráka z refluxu) a chemický (znížená tvorba slín a hladiny bikarbonátov). Dôležitá je znížená odolnosť sliznice (SO) pažeráka, porucha motorickej funkcie žalúdka, duodenostáza a zvýšenie vnútrobrušného tlaku na úroveň presahujúcu tonus LES. Medzi predisponujúce faktory patrí nadváha, tehotenstvo, nutričné faktory (zvýšená konzumácia mastných, vyprážaných jedál, čokolády, kávy, alkoholu, korenín, ovocných štiav a pod.), medikamentózna liečba (sedatíva, antidepresíva, antagonisty vápnika, anticholinergiká, β-blokátory, teofylín, nitráty, glukagón, glukokortikosteroidy).
Klinická klasifikácia GERD. Podľa medzinárodnej klasifikácie chorôb X revízie patrí GERD do kategórie K21 a delí sa na GERD s ezofagitídou (K 21.0) a GERD bez ezofagitídy (K 21.1). Pre praktickú prácu sa rozlišuje neerozívna refluxná choroba (NERD), ktorá je vo všeobecnej štruktúre GERD 60-65%, a erozívna ezofagitída (erozívna refluxná choroba) - 30-35%. NERD sa označuje, keď existuje endoskopicky negatívny variant v prítomnosti klinických údajov a údajov z ezofageálnej pH-metrie potvrdzujúcich patologické gastroezofageálne refluxy (GER) alebo podľa EFGDS katarálnu ezofagitídu. Refluxy s pH v pažeráku menej ako 4 alebo viac ako 7 trvajúce viac ako 5 minút, viac ako 50 epizód denne, s celkovým trvaním viac ako 1 hodinu a trvajúce najmenej 3 mesiace, sa považujú za patologický GER.
Na charakterizáciu refluxnej ezofagitídy sa používa klasifikácia v Los Angeles. (1994): stupeň A - jeden alebo viac defektov sliznice (SO) pažeráka s dĺžkou najmenej 5 mm, z ktorých žiadny nepresahuje viac ako 2 záhyby SO; stupeň B - jeden alebo viac defektov v sliznici pažeráka dlhších ako 5 mm, z ktorých žiadny nepresahuje viac ako 2 záhyby sliznice; Stupeň C - defekty sliznice pažeráka siahajúce do 2 alebo viacerých záhybov sliznice, ktoré spolu zaberajú menej ako 75 % obvodu pažeráka; stupeň D - defekty v sliznici pažeráka zaberajú najmenej 75 % obvodu pažeráka.
Príklad formulácie diagnózy: GERD, refluxná ezofagitída 2. stupňa závažnosti.
Klinický obraz prejavujúce sa pažerákom (pálenie záhy, odynofágia, pocit kyseliny v ústach, grganie kyslou alebo vzduchom, dysfágia, bolesť za hrudnou kosťou, na okraji xiphoidálneho výbežku, bolesť v epigastriu, škytavka, vracanie, pocit rannej sýtosti) a extraezofageálny prejavov. Medzi pažerákový prejavmi má prvoradý význam pálenie záhy, ktoré vzniká po jedle, požití sýtených nápojov, alkoholu, pri fyzickej námahe, záklone trupu alebo vo vodorovnej polohe, častejšie v noci, zastavenie užívaním minerálnej vody a antacíd. Extraezofageálne (atypické) symptómy predstavujú najmä sťažnosti naznačujúce zapojenie bronchopulmonálneho, kardiovaskulárneho systému, zubnej patológie a orgánov ENT do procesu - takzvané "masky" GERD. Značný počet pacientov so sťažnosťami charakteristickými pre srdcovú, bronchopulmonálnu, chronickú otorinolaryngologickú a zubnú patológiu sa obráti na "úzkych" špecialistov; nemusia však mať typické príznaky ezofagitídy na podozrenie na GERD.
Na bronchopulmonárne prejavov patrí chronický kašeľ, najmä nočný, obštrukčný choroba pľúc, zápal pľúc, záchvatovité spánkové apnoe. Literárne údaje poukazujú na zvýšenie rizika chorobnosti pri bronchiálnej astme a pridanie GER môže v štvrtine prípadov zhoršiť priebeh bronchiálnej astmy. Patologický GER sa považuje za spúšťač astmatických záchvatov hlavne v noci, pretože sa znižuje frekvencia prehĺtaní a zvyšuje sa účinok kyseliny na sliznicu pažeráka, čo spôsobuje rozvoj bronchospazmu v dôsledku mikroaspirácie a neuroreflexného mechanizmu.
Diagnostická stratégia lekára primárnej starostlivosti pre chronický kašeľ: nevyhnutné vylúčenie pacienta užívajúceho inhibítory angiotenzín-konvertujúceho enzýmu a fajčenie, rádiografia dýchacieho systému; má sa vykonať vyšetrenie ORL orgánov, rádiografia paranazálnych dutín, spirografia s bronchodilatátorom, EFGDS a 24-hodinová pH-metria.
na kardiovaskulárne prejavov GERD označuje bolesť na hrudníku podobnú angíne pectoris v dôsledku hypermotorickej dyskinézy pažeráka (sekundárny spazmus pažeráka).
Klinické príznaky bolesti na hrudníku spojené s refluxom: sú pálivého charakteru, lokalizované za hrudnou kosťou, nevyžarujú, sú spojené s príjmom potravy, prejedaním, diétnymi chybami, vyskytujú sa pri zmene polohy tela (náklony, horizontálna poloha), klesajú po užití alkalických minerálnych vôd, antacíd alebo antisekrečných liekov, v kombinácii s pálením záhy a/alebo dysfágiou. Keďže srdcová „maska“ GERD je sprostredkovaná cez n. vagus, kardialgia sa často kombinuje s prejavmi autonómnej dysfunkcie – tachyarytmia, pocit tepla a zimnica, závraty, emočná labilita. Diferenciálna diagnóza sa robí s koronárnou chorobou srdca (ICHS) a jej prejavom - angínou pectoris, trvanie bolesti je 1-2 minúty, bolesť má charakteristické ožiarenie, je vyvolaná fyzickou aktivitou a je zastavená nitroglycerínom. Verifikácia IHD zahŕňa koronárnu angiografiu, EKG Holterov monitoring, bicyklovú ergometriu, záťažovú ECHO kardiografiu.
Otolaryngologické Príznaky GERD sú najpočetnejšie a najrozmanitejšie. Patria sem pocit bolesti, kóma, cudzie teleso v hrdle, bolesť hrdla, túžba „vykašľať sa“, chrapot, záchvatovitý kašeľ. Okrem toho môže GERD spôsobiť rekurentnú sinusitídu, zápal stredného ucha, faryngitídu, laryngitídu, ktorá nie je vhodná pre štandardnú liečbu. Mechanizmus vzniku týchto symptómov je spojený s faryngolaryngeálnym refluxom, ktorého príčinou je GER, prenikajúci proximálne cez horný pažerákový zvierač.
Zubnú „masku“ predstavuje pálenie jazyka, líc, zhoršené chuťové vnemy, patologická deštrukcia zubnej skloviny a opakujúce sa kazy.
U 10 – 20 % pacientov s GERD sa vyvinie Barrettov pažerák, získaný stav, ktorý je komplikáciou GERD, ktorá sa vyvinie v dôsledku nahradenia zničeného vrstveného dlaždicového epitelu spodnej časti pažeráka cylindrickým epitelom (Barrettov epitel) , čo predisponuje k rozvoju adenokarcinómu pažeráka. Rizikové faktory pre rozvoj Barrettovho pažeráka: pálenie záhy viac ako 2-krát týždenne, mužské pohlavie, trvanie príznakov viac ako 5 rokov.
Diagnóza GERD je postavená predovšetkým na základe sťažností pacientov a inštrumentálne metódy (EFGDS, 24-hodinová pH-metria) sú doplnkové alebo potvrdzujúce diagnózu. Podľa klinických usmernení povinné laboratórne testy zahŕňajú kompletný krvný obraz, moč, krvnú skupinu, Rh faktor. Inštrumentálne metódy výskumu: raz EFGDS, biopsia sliznice pažeráka pri komplikovanom GERD (vredy, striktúry, Barrettov pažerák), RTG vyšetrenie pažeráka a žalúdka pri podozrení na hiátovú herniu, striktúru, adenokarcinóm pažeráka. NERD), biopsia sliznice pažeráka pri komplikovanej GERD. Pre ďalšie metódy zahŕňajú 24-hodinovú intraezofageálnu pH-metriu, intraezofageálnu manometriu, ultrazvuk brucha, EKG, bicyklovú ergometriu, test inhibítora protónovej pumpy (PPI test). Možnosť a účelnosť vykonania testu PPI je spôsobená vysokou prevalenciou NERD a môže zohrávať úlohu skríningu: nedostatok účinku alebo rýchly návrat symptómov po vysadení PPI núti zamyslieť sa nad potrebou ďalších výskumných metód (endoskopia pH-metria atď.).
Odlišná diagnóza vykonávané s peptickým vredom a striktúrou pažeráka, gastroezofageálnym karcinómom, divertikulom pažeráka, achaláziou kardie, achaláziou a spazmom perofaryngeálneho svalu, faryngoezofageálnou dyskinézou, idiopatickým difúznym ochorením pažeráka, primárnym arteriálnym dyskinéznym pažerákom ako spazmóza pažeráka ina pectoris, infarkt myokardu), bronchopulmonálna patológia her, ochorenia ORL -org.
Vzhľadom na špecifiká práce lekára prvého kontaktu, najmä praktického lekára, je potrebné zamerať sa na diferenciálnu diagnostiku jedného z hlavných príznakov ochorení pažeráka - dysfágia(ťažkosti s prehĺtaním, pocit, že jedlo je blokované v prechode cez ústa do hltana alebo pažeráka). Prideľte orofaryngeálnu a ezofageálnu dysfágiu.
Orofaryngeálna dysfágia je charakterizovaná porušením toku potravy do pažeráka a je sprevádzaná spätným tokom potravy do úst alebo nosa. Patogenetické mechanizmy takejto dysfágie zahŕňajú slabosť priečne pruhovaných svalov zapojených v počiatočnom štádiu prehĺtania, neschopnosť uzavrieť nosohltan a hrtan, neúplnú relaxáciu horného pažerákového zvierača. Pacient sa dusí, kašle, špliecha slinami, musí vynaložiť úsilie na úspešné prehĺtanie, je možná aspirácia. Takáto dysfágia sa môže vyskytnúť v dôsledku neurologických a neuromuskulárnych ochorení, ktoré narúšajú prehĺtanie: mŕtvice, roztrúsená a amyotrofická laterálna skleróza, botulizmus, parkinsonizmus, bulbárna obrna, poliomyelitída, syringomyelia, myasthenia gravis, myopatia, diabetes mellitus a alkoholizmus ako prejav neuropatie. Niektoré kolagenózy (dermatomyozitída) v dôsledku poškodenia priečne pruhovaných svalov môžu tiež spôsobiť dysfágiu. Príčinou orofaryngeálnej dysfágie môžu byť aj zápalové ochorenia: akútna faryngitída, ktorá spôsobuje bolesť a opuch v hrdle, čo dočasne sťažuje prehĺtanie. Zriedkavejšie príčiny orofaryngeálnej dysfágie sú rakovina hrtana, paratonsilárny absces, parotitída, akútna tyroiditída, orofaryngeálne radiačné poškodenie. S malformáciami hltana a pažeráka môže byť dysfágia spojená so Zenkerovým divertikulom dolného hltana, čo sa vyskytuje u starších ľudí, ktorí sa sťažujú na ťažké a bolestivé prehĺtanie, pretrvávajúci kašeľ a niekedy opuch na bočnom povrchu krku, ktorý sa znižuje s regurgitáciou jedlo a hlien. Idiopatická dysfunkcia krikofaryngeálneho svalu je podozrivá z porušenia príjmu potravy, keď nie sú zistené neurologické, degeneratívne alebo zápalové procesy v hltane a pažeráku.
Ezofageálna dysfágia pozorované počas normálneho prehĺtania, ale so zhoršeným prechodom tuhej alebo tekutej potravy cez pažerák do žalúdka a je charakterizované objavením sa 2-5 sekúnd po prehltnutí potravy pocitu plnosti, „kómy“ a bolesti za chrbtom hrudná kosť. Mnoho pacientov dokáže presne určiť úroveň retencie bolusu potravy. Existujú dve skupiny patologických stavov, ktoré spôsobujú dysfágiu pažeráka. Ide o poruchy motility pažeráka (motorická dysfágia) a mechanické zúženie jeho lúmenu (mechanická dysfágia) . Motorická dysfágia nastáva pri príjme tuhej aj tekutej stravy a je charakterizovaná pálením záhy, bolesťou na hrudníku pripomínajúcou angínu, aspiráciou, stratou hmotnosti a často regurgitáciou. Príčiny tohto typu dysfágie sú achalázia, difúzny spazmus pažeráka, sklerodermia pažeráka. Mechanická dysfágia je spôsobená faktormi vedúcimi k zmene lúmenu pažeráka: vnútorné zúženie alebo vonkajšia kompresia. Mechanickú dysfágiu najčastejšie spôsobuje spinocelulárny karcinóm pažeráka a jeho metastatické lézie (častejšie - rakovina prsníka, rakovina pľúc, lymfómy a leukémie), peptické a iné nezhubné zúženia pažeráka, spôsobujúce progresívnu dysfágiu, ktorá vzniká najmä pri snaží prehĺtať tuhú stravu a klesá pri zapíjaní potravy vodou. Príčina dysfágie môže byť aj infekčná, najmä kandidová a herpetická ezofagitída, ktorá často prebieha bez poškodenia ústnej dutiny. Kandidová ezofagitída sa častejšie vyvíja s výrazným oslabením imunitného systému: u ľudí užívajúcich antibiotiká, glukokortikoidy a u pacientov s diabetes mellitus. Pravidelné ťažkosti s prehĺtaním tuhej potravy sú niekedy skorým príznakom zúženia lúmenu v oblasti pažerákovo-žalúdočnej anastomózy v dôsledku tvorby hlienového prstenca (Schatského prstenec). Dysfágia je intermitentná, typicky sa objavuje pri prehĺtaní mäsa – takzvaný „steakový syndróm“. Zrasty spojivového tkaniva v cervikálnom pažeráku v kombinácii s nedostatkom železa a iných látok v potrave (Plummer-Vinsonov alebo Paterson-Kelly syndróm), spojené so zvýšeným rozvojom spinocelulárneho karcinómu pažeráka a hltana, môžu tiež spôsobiť dysfágiu. Patogenéza tohto syndrómu je nejasná, ale často sa upraví doplnením železa a korekciou inej podvýživy, a to aj bez deštrukcie membrány. Poruchy prehĺtania v dôsledku dysfunkcie pažeráka sa pozorujú pri mnohých systémových ochoreniach - Crohnova choroba, sarkoidóza, Behcetova choroba, pemfigoid a vezikulárna epidermolýza. Zriedkavo sa dysfágia objavuje po kmeňovej vagotómii alebo po fundoplikácii pri refluxnej ezofagitíde.
Príčinou dysfágie môže byť stlačenie pažeráka zvonku krvnými cievami - s atypickým výtokom pravej podkľúčovej tepny.
Globus hystericus sa považuje za prejav dysfágie hysterického pôvodu a prejavuje sa ako pocit hrče zaseknutej v hrdle. Pri skutočnom vykonávaní aktu prehĺtania však nie sú pozorované žiadne ťažkosti. V niektorých prípadoch je výskyt tohto príznaku spojený buď s prítomnosťou zóny regionálnej parestézie, alebo s rozvojom laryngofaryngeálneho alebo pažerákového spazmu.
Indikácie pre hospitalizáciu. Pacienti sú hospitalizovaní na antirefluxnú liečbu s komplikovaným priebehom ochorenia, ako aj s neúčinnosťou adekvátnej liekovej terapie, na chirurgickú intervenciu (fundoplikáciu) s neúčinnosťou liekovej terapie a endoskopických alebo chirurgických zákrokov v prítomnosti komplikácií ezofagitídy: striktúra, Barrettov pažerák, krvácanie.
Liečba. Cieľom terapie GERD je zmiernenie klinických symptómov, hojenie erózií, zlepšenie kvality života, prevencia alebo eliminácia komplikácií a prevencia relapsov. Liečba zahŕňa predovšetkým nefarmakologické metódy.
Zásahy do životného štýlu: odvykanie od fajčenia, normalizácia telesnej hmotnosti, diéta s vylúčením pikantných, kyslých, mastných jedál, korenín, potravín, ktoré spôsobujú tvorbu plynov, sýtených nápojov, kávy, alkoholu, čokolády, cibule, cesnaku, paradajok, citrusových plodov. Pacientom je potrebné odporučiť, aby jedli najneskôr niekoľko hodín pred spaním, po jedle by si 1,5-2 hodiny nemali ľahnúť, nosiť tesné oblečenie a pevné opasky, vylúčiť cvičenie s ohybmi nadol.Pacientom treba odporučiť, aby užívať podľa možnosti lieky, ktoré nepriaznivo pôsobia na sliznicu pažeráka a znižujú tonus LES: nitráty, antagonisty vápnika, spazmolytiká, progesterón, antidepresíva, teofylín, nesteroidné protizápalové lieky a tiež zvýšiť hlavovú časť posteľ o 15-20 cm.
Drogová terapia pre GERD stanovuje vymenovanie troch skupín liekov: antisekrečné činidlá, antacidá a prokinetiká. Podľa Bellovho pravidla k hojeniu erózií pažeráka dochádza v 80-90% prípadov, ak je možné udržať pH v pažeráku> 4 počas dňa aspoň 16-22 hodín. Preto sú inhibítory protónovej pumpy (PPI) prvou voľbou. V súlade s klinickými usmerneniami pre gastroenterológiu dĺžka liečby erozívnej refluxnej choroby závisí od štádia ochorenia. Pri jednotlivých eróziách (štádiá A a B) sa liečba vykonáva 4 týždne, pri viacnásobných eróziách - (štádiá C a D) - 8 týždňov. Aplikujte omeprazol 20-40 mg/deň, lansoprazol 30-60 mg/deň, rabeprazol 20 mg/deň, pantoprazol 40-80 mg/deň, esomeprazol 40 mg/deň. Dvojitá dávka PPI alebo predĺženie trvania liečby (až na 12 týždňov a viac) je potrebné, ak hojenie erózií nie je dostatočne rýchle alebo pri extraezofageálnych prejavoch. Podporná liečba erozívnych foriem GERD sa vykonáva v štandardnej alebo polovičnej dávke počas 26 týždňov a pri komplikovanom priebehu ochorenia - počas 52 týždňov. V prípade NERD sa IPP raz denne (omeprazol 20 mg, lansoprazol 30 mg, pantoprazol 20–40 mg, rabeprazol 20 mg, ezomeprazol 20 mg) podávajú raz denne počas 4–6 týždňov. Ďalšia liečba sa vykonáva v štandardnej alebo polovičnej dávke v režime "na požiadanie". Použitie blokátorov H-2 je menej účinné.
Antacidá sa používajú ako symptomatický liek na zmiernenie zriedkavého pálenia záhy, 15 ml suspenzie 3-krát denne 1,5 hodiny po jedle a na noc až do zmiernenia príznakov (priemer 2 týždne). V prípade refluxnej ezofagitídy s refluxom pažeráka duodenálneho obsahu sa podľa klinických odporúčaní používa kyselina ursodeoxycholová 250-350 mg / deň. v kombinácii s prokinetikami. Terapia na požiadanie – užívanie PPI, keď sa objavia príznaky GERD – sa používa pri endoskopicky negatívnej refluxnej chorobe.
Vzhľadom na trvanie antisekrečnej terapie sa treba pozastaviť aj nad možnými vedľajšími účinkami PPI. V dôsledku výrazného zníženia bariérových vlastností žalúdočnej šťavy sa vytvárajú podmienky pre rozvoj podmienene patogénnej flóry v proximálnej aj distálnej časti gastrointestinálneho traktu. Zvýšené riziko črevných infekcií, vrátane hnačky súvisiacej s Clostridium difficile. V podmienkach ťažkej hypochlórhydrie sa vyvíja migrácia H. pylori z antrum do tela žalúdka s tvorbou atrofickej gastritídy, ktorá je prvým krokom kaskády Correa. V tejto súvislosti by všetci pacienti s GERD s dlhodobým užívaním PPI mali byť vyšetrení na H. pylori a ak je výsledok pozitívny, podstúpiť eradikačnú terapiu. Množstvo štúdií poukazuje na častejší výskyt infekcií dýchacieho systému so závažnou supresiou kyseliny. Ukázalo sa tiež, že dlhodobé užívanie PPI zvyšuje riziko osteoporotických zlomenín, čo pravdepodobne súvisí s malabsorpciou vápnika. Užívanie vysokých dávok PPI dlhšie ako rok zvyšuje riziko zlomenín bedra 1,9-krát. Niektoré zdroje uvádzajú rozvoj hepatopatie pri dlhodobom užívaní PPI. Medzi nežiaduce účinky PPI patrí zníženie intragastrickej koncentrácie vitamínu C, najmä v biologicky aktívnej forme antioxidantov, ako aj vplyv PPI na vakuolárnu H + -ATPázu, ktorá podmieňuje mnohé biochemické procesy v ľudskom organizme. Preto aj napriek nepochybnej účinnosti IPP pri liečbe GERD treba brať do úvahy jeho možný negatívny vplyv na ľudské zdravie vo všeobecnosti. Prokinetika ("Cerucal", "Domperidon", "Cisaprid", "Itoprid") zvyšujú tón dolného pažerákového zvierača, urýchľujú evakuáciu zo žalúdka, zvyšujú klírens pažeráka, používajú sa v kombinácii s liekmi z iných skupín; niektoré prokinetiká (cisaprid) majú obmedzené použitie v dôsledku kardiotoxicity.
Edukácia pacienta. Práve lekár prvého kontaktu - praktický lekár, lokálny terapeut zohráva veľkú úlohu pri edukácii pacienta, vykonávaní sanitárnej a výchovnej práce. Organizácia „Škôl pacientov s GERD“ je racionálna. Pacienti sa učia, že GERD je chronické ochorenie, ktoré si vyžaduje dlhodobú udržiavaciu terapiu PPI, aby sa predišlo komplikáciám. Aktívne vysvetlite dôležitosť nemedikamentóznej liečby GERD a zásahov do životného štýlu. Pacientov je potrebné informovať o možných komplikáciách GERD a „úzkostných symptómoch“: progresívna dysfágia alebo odynofágia, krvácanie, chudnutie, kašeľ alebo astmatické záchvaty, bolesť na hrudníku, časté vracanie. Pacientom s dlhotrvajúcimi nekontrolovanými príznakmi refluxu by sa mala vysvetliť potreba endoskopie na zistenie komplikácií (Barrettov pažerák), a ak sú prítomné, potreba pravidelného EFGDS s biopsiou a histologickým vyšetrením.
Hlavnými problémami pri liečbe GERD je potreba predpisovať veľké dávky antisekrečných liekov a vykonávať dlhodobú hlavnú (najmenej 4-8 týždňov) a udržiavaciu (6-12 mesiacov) terapiu. Ak tieto podmienky nie sú splnené, pravdepodobnosť recidívy ochorenia je veľmi vysoká. Početné štúdie ukázali, že u 80 % pacientov, ktorí nedostávajú adekvátnu udržiavaciu liečbu, sa v priebehu nasledujúcich 26 týždňov rozvinie relaps a do jedného roka je pravdepodobnosť relapsu 90 – 98 %. Od lekára prvého kontaktu sa teda vyžaduje komplexný prístup k manažmentu pacientov s GERD, ktorý zabezpečí účinnosť terapie, trpezlivosť a vytrvalosť. Mimoriadne dôležitá je edukácia pacientov, vrátane nefarmakologických spôsobov liečby.
L.T. Pimenov, T.V. Savelyeva
Iževskštátlekárskeakadémie
Pimenov Leonid Timofeevič — doktor lekárskych vied, profesor,
Prednosta Kliniky všeobecného lekára a vnútorného lekárstva s kurzom urgentnej medicíny
Literatúra:
1. Kalinin A.V. Ochorenia horného gastrointestinálneho traktu závislé od kyseliny. Lieková korekcia porúch sekrécie. Klinické perspektívy v gastroenterológii, hepatológia 2002; 2:16-22.
2. Isakov V.A. Epidemiológia GERD: Východ a Západ. Expert. a klin. gastroenterológia. 2004; 5:2-6.
3. Lundell L. Pokroky v stratégiách liečby gastroezofageálnej refluxnej choroby. Postgraduálny kurz EAGE. Ženeva, 2002. S. 13-22.
4. Maev I.V., Trukhmanov A.S. Neerozívna refluxná choroba z pohľadu modernej gastroenterológie: klinické príznaky a vplyv na kvalitu života pacientov. Ruský lekársky časopis 2004; 12(23): 1344-1348.
5. Kalinin A.V. Ochorenia horného gastrointestinálneho traktu závislé od kyseliny. Lieková korekcia porúch sekrécie. Klinické perspektívy v gastroenterológii, hepatológia 2002; 2:16-22.
6. Lazebnik L.B., Bordin D.S., Masharova A.A.,b Spoločnosť proti páleniu záhy. Experimentálna a klinická gastroenterológia 2007; 4:5-10.
7. Roshina T.V. Gastroezofageálna refluxná choroba u pacientov s bronchiálnou astmou: Abstrakt práce. diplomová práca ... cand.med.sci. M., 2002. 21 str.
8. Ivaškin V.T. Gastroenterológia: klinické usmernenia. Ed. V.T. Ivaškin. 2. vydanie, rev. a dodatočné M.: GEOTAR-Media, 2009. 208 s.
9. Vakil N., van Zanten S.V., Kahrilas P., Dent J., Jones R. a Global Consensus Group. Montrealská definícia a klasifikácia gastroezofageálnej refluxnej choroby: globálny konsenzus založený na dôkazoch. Am. J. Gastroenterol. 2006; 101: 1900-1920.
10. Ivashkin V.T., Sheptulin A.A. Diagnostika a liečba gastroezofageálneho refluxu: príručka pre lekárov. M., 2005. 30 s.
11. Maev I.V., Samsonov A.A., Trukhmanov A.S., et al Pozitívne skúsenosti s použitím antacida Maalox u pacientov s novodiagnostikovanou neerozívnou refluxnou chorobou. Ruský lekársky časopis 2008; 2:50-55.
13. Stremoukhov A.A. Hlavné príznaky chorôb pažeráka. Bulletin rodinného lekárstva 2005; 2 (04): 12-17.
14. Targownic L.E., Lix L.M., prior H.J. Použitie inhibítorov protónovej pumpy a riziko zlomenín súvisiacich s osteoporózou. Can Med Assoc J 2008; 179:319-326.
 Staroveké a veľmi zvláštne športové Pištoľový súboj
Staroveké a veľmi zvláštne športové Pištoľový súboj Najstarší šport na svete
Najstarší šport na svete Vladimir Kolokoltsev: služba v Afganistane, boj proti skupinám organizovaného zločinu a ďalšie fakty z biografie vedúceho ministerstva vnútra
Vladimir Kolokoltsev: služba v Afganistane, boj proti skupinám organizovaného zločinu a ďalšie fakty z biografie vedúceho ministerstva vnútra Pestúnska škola
Pestúnska škola Super jasné LED diódy. Typy a zariadenia. Práca a aplikácia. Výber, použitie a vlastnosti LED diód: užitočné informácie a profesionálne odporúčania LED super jasná výkonná biela
Super jasné LED diódy. Typy a zariadenia. Práca a aplikácia. Výber, použitie a vlastnosti LED diód: užitočné informácie a profesionálne odporúčania LED super jasná výkonná biela Všetky ženy sú ako ženy a ja som blázon za milión A hlavná otázka znie: aká žena na to potrebuje byť
Všetky ženy sú ako ženy a ja som blázon za milión A hlavná otázka znie: aká žena na to potrebuje byť Elsa scarlett titania. Prezbrojenie Elsy. Tajomstvo srdca Erzy Scarlett
Elsa scarlett titania. Prezbrojenie Elsy. Tajomstvo srdca Erzy Scarlett